Myosin: Aufbau, Funktion in eukaryotischen Zellen und Muskelkontraktion
Myosin: Aufbau, Funktionen in eukaryotischen Zellen und Rolle bei Muskelkontraktion erklärt — Struktur, ATP‑abhängiger Mechanismus, Typen und biologische Bedeutung kompakt erklärt.
Myosine sind eine Familie spezialisierter Proteinen, die vor allem für die Muskelkontraktion und verschiedene Bewegungsprozesse in eukaryotischen Zellen verantwortlich sind. Myosine benötigen ATP als Energiequelle, um mechanische Arbeit zu leisten. In Eukaryonten wurde eine große Zahl unterschiedlicher Myosin-Gene gefunden; diese Vielfalt spiegelt die breite Palette zellulärer Aufgaben wider, bei denen Myosine eine Rolle spielen.
Die grundlegende Struktur und die grundlegende Funktion des Myosins sind über viele Arten hinweg stark konserviert: so kann beispielsweise das Myosin II aus Kaninchenmuskeln an Aktinfilamente einer Amöbe binden und mechanische Arbeit verrichten. Trotz dieser Konservierung haben verschiedene Myosin-Klassen spezifische Anpassungen, die sie für unterschiedliche Aufgaben in der Zelle geeignet machen.
Aufbau eines Myosinmoleküls
Ein typisches Myosinmolekül besteht aus drei funktionellen Bereichen:
- Motor- oder Kopfdomäne: Bindet an Aktin und enthält die ATPase-Aktivität, die ATP hydrolysiert und so Energie für die Konformationsänderungen liefert.
- Hals- oder Hebelarm: Trägt an diesen Stellen leichte Ketten (light chains) und wirkt als Hebel, der die kleine Konformationsänderung im Kopf in eine größere Bewegung übersetzt. Die Länge des Hebelarms beeinflusst die Schrittweite des Myosins.
- Schwanzdomäne: Vermittelt Dimerisierung, Bündelbildung oder die Bindung an weitere Proteine bzw. Fracht. Bei manchen Klassen (z. B. Myosin II) ermöglichen tail-Regionen die Bildung von dickeren Filamenten.
Myosin-Klassen und Eigenschaften
Myosine werden in zahlreiche Klassen (z. B. Myosin I, II, V, VI usw.) eingeteilt. Wichtige Unterschiede sind:
- Myosin II: Bildet bipolar organisierte Filamente (dicke Filamente) und ist der Haupttyp in Skelett-, Herz- und glatter Muskulatur. Verantwortlich für die klassische Muskelkontraktion.
- Myosin V: Prozessives Motorprotein, das längere Schritte entlang von Aktinfilamenten macht und Organellen- bzw. Vesikeltransport gewährleistet.
- Myosin VI: Besonders, weil es sich entgegen der üblichen Richtung entlang des Aktins (zum Minus-Ende) bewegt.
- Weitere Klassen übernehmen spezialisierte Aufgaben z. B. in der Sinnesepithelfunktion (Hörsinn), Zelladhäsion oder Signalübertragung.
Mechanismus: ATP-Zyklus und Kraftschlag
Der mechanische Zyklus eines Myosinkopfes umfasst mehrere Zustände:
- ATP-Bindung an den Myosinkopf führt zur Ablösung vom Aktin.
- ATP-Hydrolyse (zu ADP + Pi) versetzt den Kopf in eine „gespannte“ Konformation.
- Wiederbindung an Aktin und anschließend Freisetzung von Pi löst den eigentlichen Kraftschlag (Power Stroke) aus — der Hebelarm schwenkt und erzeugt Verschiebung relativ zum Aktinfilament.
- Abschließend wird ADP freigesetzt, und ein neuer ATP-Bindungszyklus beginnt.
Die Umsetzung von chemischer Energie (ATP) in mechanische Arbeit folgt dem Hebelarm-Modell: kleine strukturelle Änderungen der Kopfdomäne werden durch den Hebelarm verstärkt und resultieren in einer gerichteten Bewegung.
Rolle in der Muskelkontraktion
In Skelett- und Herzmuskulatur sind Aktin- und Myosinfilamente in Sarkomeren organisiert. Die Kontraktion beruht auf dem gleitenden Filamentmodell:
- Myosin-II-Köpfe binden wiederholt an Aktin und „ziehen“ die dünnen Filamente Richtung Mitte des Sarkomers — dadurch verkürzen sich die Sarkomere und der Muskel kontrahiert.
- Die Kontraktion wird durch Ca2+-abhängige Regulation gesteuert: Bei erhöhtem intrazellulärem Ca2+ bindet Ca2+ an das Troponin-Komplex, wodurch Tropomyosin die Blockade der Bindungsstellen auf Aktin freigibt und Myosinbindungsstellen zugänglich werden.
- In glatten Muskeln wird zusätzlich die Phosphorylierung der regulatorischen leichten Kette von Myosin durch Myosin-Leichtketten-Kinase (MLCK) reguliert.
Weitere Funktionen in eukaryotischen Zellen
Abgesehen von der Muskelkontraktion übernehmen Myosine zahlreiche zelluläre Aufgaben:
- Intrazellulärer Transport von Organellen, Vesikeln und mRNA (z. B. Myosin V).
- Zellmigration und Umbau des Zytoskeletts durch Wechselwirkung mit Aktin.
- Zellteilung (Cytokinese): Myosin II bildet mit Aktin den kontraktilen Ring, der Tochterzellen trennt.
- Mechanotransduktion und Verankerung von Zelladhäsionsstrukturen.
Regulation und klinische Bedeutung
Myosinaktivität wird auf mehreren Ebenen reguliert: Genexpression unterschiedlicher Myosin-Isoformen, posttranslationale Modifikationen (z. B. Phosphorylierung der regulatorischen Leichteinheiten), sowie Interaktion mit adaptiven Proteinen. Fehlfunktionen oder Mutationen können zu Krankheiten führen, beispielsweise:
- Erblich bedingte Kardiomyopathien durch Mutationen in β-Myosin-Heavy-Chain (bei Menschen).
- Hör- und Sehbehinderungen, wenn für spezielle Myosinklassen relevante Gene mutiert sind (z. B. Myosin VIIa bei Usher-Syndrom).
Evolutionäre Konservierung
Die Struktur und die Grundmechanik der Myosinmotoren sind über viele Arten hinweg konserviert. So lässt sich funktionelle Kompatibilität zwischen entfernten Organismen beobachten — ein Hinweis auf die fundamentale Bedeutung dieses Motorproteins für zelluläre Bewegungsprozesse.
Zusammenfassend sind Myosine vielseitige Motorproteine mit klarer Spezialisierung: Vom Aufbau (Kopf–Hals–Schwanz) über den ATP-getriebenen Kraftschlag bis hin zu ihrer Regulation und vielfältigen biologischen Rollen — sie sind Schlüsselkomponenten für Bewegung und Organisation in eukaryotischen Zellen.
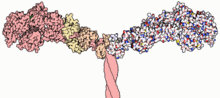
Teil der Myosin II-Struktur
Aufbau und Funktion
Teile
Die meisten Myosinmoleküle setzen sich aus einem Kopfteil, einem Halsteil und einem Schwanzteil zusammen.
- Der Kopfteil greift nach dem Aktin und nutzt die Energie von ATP zum Ziehen, wodurch der Muskel kürzer wird.
- der Halsteil als Hebel wirkt.
- Der Schwanzteil interagiert meist mit anderen Molekülen oder anderen Myosin-Untereinheiten. In einigen Fällen kann der Schwanzteil helfen, die Bewegung zu regulieren.
Krafthub
Viele Myosinmoleküle können Muskeln kürzer machen, indem sie die Energie nutzen, die beim Aufspalten von ATP-Molekülen in ADP und eine Phosphatgruppe freigesetzt wird. Der Kraftschlag entsteht, wenn ein Phosphat, das n abgebrochen wurde, aus dem Myosin freigesetzt wird. Dadurch verändert das Myosin seine Form, so dass es gegen das Aktin zieht. Wenn das ADP-Molekül freigesetzt wird und sich ein neues ATP-Molekül an den Myosinkopf anschließt, löst sich der Kopf vom Aktin. Das Myosin bricht das neue ATP und der Zyklus geht weiter. Durch die kombinierte Wirkung aller Kraftschläge der verschiedenen Myosinmoleküle wird der Muskel kürzer.
Suche in der Enzyklopädie