Das Boyle'sche Gesetz (auch Mariottes Gesetz und das Boyle-Mariotte-Gesetz genannt) ist ein Gesetz über ideale Gase.
Das Gesetz kann wie folgt formuliert werden:
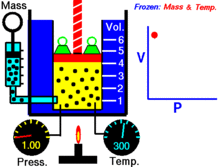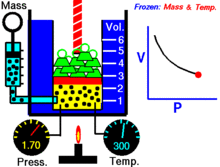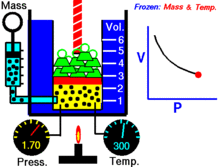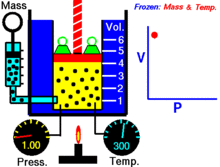
Bei einer festen Menge eines idealen Gases, das auf einer festen Temperatur gehalten wird, sind P (Druck) und V (Volumen) umgekehrt proportional.
Mit anderen Worten, das Volumen einer konstanten Masse eines idealen Gases bei konstanter Temperatur ist umgekehrt proportional zum Druck, der auf dieses Gas ausgeübt wird.
In Symbolen ist das Gesetz:
P ∝ 1 V {\displaystyle P\propto {\frac {\frac {1}{V}}}}
oder
P V = k {\Anzeigestil PV=k}
wobei P der Druck des Gases, V das Volumen des Gases und k eine Konstante ist.
Für eine gegebene Gasmasse bei konstanter Temperatur ist das Produkt aus Druck und Volumen eine Konstante. Wenn das Volumen abnimmt, nimmt der Druck proportional zu und umgekehrt. Wenn sich zum Beispiel der Druck halbiert, verdoppelt sich das Volumen.
Angenommen, Sie haben einen Tank, der ein bestimmtes Gasvolumen bei einem bestimmten Druck enthält. Wenn Sie das Volumen des Tanks verringern, befindet sich nun die gleiche Anzahl von Gasteilchen in einem kleineren Raum. Daher erhöht sich die Anzahl der Kollisionen. Daher ist der Druck größer.
Stellen Sie sich vor, Sie haben ein Gas mit einem bestimmten Druck (P1) und Volumen (V1). Wenn Sie den Druck auf einen neuen Wert (P2) ändern, ändert sich das Volumen auf einen neuen Wert (V2). Wir können das Boyle'sche Gesetz verwenden, um beide Sätze von Bedingungen zu beschreiben:
P 1 V 1 = k {\Anzeigestil P_{1}V_{1}=k}
P 2 V 2 = k {\Anzeigestil P_{2}V_{2}=k}
Die Konstante k ist in beiden Fällen die gleiche, so dass wir Folgendes sagen können:
P 1 V 1 = P 2 V 2 {\Anzeigestil P_{1}V_{1}=P_{2}V_{2}}}
Beispiel: Der Druck eines Gases beträgt 3 atm und das Volumen 5 Liter. Wenn der Druck auf 2 atm reduziert wird, wie gross ist das Volumen?
P 1 V 1 = P 2 V 2 {\Anzeigestil P_{1}V_{1}=P_{2}V_{2}}}
V 2 = P 1 V 1 P 2 {\Anzeigestil V_{2}={\frac {P_{1}V_{1}}}{P_{2}}}}
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}{2}}}}
V 2 = 15 2 {\darstellungsstil V_{2}={\frac {15}{2}}}}
V 2 = 7,5 {\Anzeige-Stil V_{2}=7,5}
∴ Das Volumen wird 7,5 Liter betragen.
Das Gesetz wurde 1662 von Robert Boyle und danach 1679 von Edme Mariotte unabhängig voneinander gefunden.