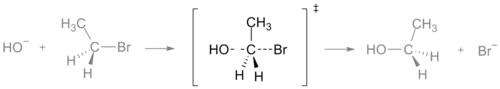Bei einer chemischen Reaktion ist der Übergangszustand der Punkt, an dem ein maximaler Energiewert vorliegt. Diese Energie wird als Aktivierungsenergie bezeichnet. Wenn zwei oder mehr Moleküle gemischt werden, treffen sie aufeinander. Wenn sie mit genügend Energie auftreffen, um den Übergangszustand zu durchlaufen, reagieren sie und bilden neue Moleküle. Im Übergangszustand werden neue Bindungen gebildet, während die alten gebrochen werden. In einem Diagramm oder einer Zeichnung wird der Übergangszustand oft mit dem Doppel-Dolch-Symbol ‡ gekennzeichnet.
Es ist sehr schwierig, einen Übergangszustand zu studieren. Das liegt daran, dass er eine so hohe Energie hat, dass die Moleküle für eine sehr kurze Zeit, normalerweise Femtosekunden, in dieser Form bleiben. Es ist wichtig, Übergangszustände nicht mit Zwischenprodukten zu verwechseln. Zwischenprodukte befinden sich an Punkten mit minimaler Energie und können sehr lange leben. Wie ein Übergangszustand befindet sich ein Zwischenprodukt jedoch zwischen Reagenzien und Produkten einer Reaktion.
Die Untersuchung von Übergangszuständen ist sehr wichtig, um Reaktionsmechanismen zu verstehen. Es gibt Theorien und Computerprogramme, mit denen man berechnen kann, wie der Übergangszustand aussieht. Dies ist ein Teil der chemischen Kinetik.