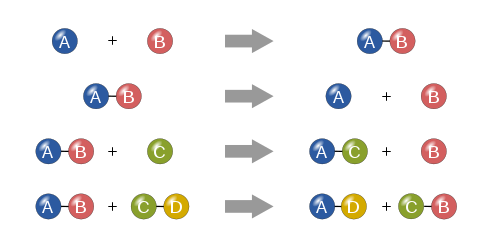
Eine chemische Reaktion findet statt, wenn eine oder mehrere Chemikalien in eine oder mehrere andere Chemikalien umgewandelt werden. Beispiele:
- Eisen und Sauerstoff verbinden sich zu Rost
- Kombination von Essig und Backpulver zur Herstellung von Natriumacetat, Kohlendioxid und Wasser
- Dinge, die brennen oder explodieren
- viele Reaktionen, die im Inneren von Lebewesen stattfinden
- elektrochemische Reaktionen beim Entladen oder Wiederaufladen von Batterien
Einige Reaktionen sind schnell, andere langsam. Einige geschehen mit unterschiedlichen Geschwindigkeiten, abhängig von der Temperatur oder anderen Dingen. Zum Beispiel reagiert Holz nicht mit Luft, wenn es kalt ist, aber wenn man es heiß genug macht, fängt es an zu brennen. Einige Reaktionen geben Energie ab. Dies sind exotherme Reaktionen. Bei anderen Reaktionen wird Energie aufgenommen. Dies sind endothermeReaktionen.
Kernreaktionen sind keine chemischen Reaktionen. An chemischen Reaktionen sind nur die Elektronen der Atome beteiligt; an Kernreaktionen sind die Protonen und Neutronen in den Atomkernen beteiligt.
Was bei einer chemischen Reaktion passiert
Bei einer chemischen Reaktion werden chemische Bindungen gebrochen und neue Bindungen gebildet. Dabei werden die Atome neu angeordnet, aber die Gesamtzahl der Atome (und damit die Masse) bleibt erhalten — das nennt man Gesetz der Massenerhaltung. Chemische Reaktionen werden oft durch chemische Gleichungen beschrieben, die Edukte (Ausgangsstoffe) links und Produkte rechts zeigen, mit stöchiometrischen Koeffizienten, die das Mengenverhältnis angeben.
Faktoren, die die Reaktionsgeschwindigkeit beeinflussen
- Temperatur: Höhere Temperatur erhöht die Teilchengeschwindigkeit und damit meist die Reaktionsrate.
- Konzentration: Größere Konzentrationen der Reaktanten führen meist zu mehr Zusammenstößen pro Zeit und damit zu schnelleren Reaktionen.
- Oberfläche: Feststoffe reagieren schneller, wenn sie feiner verteilt sind (größere Oberfläche).
- Druck: Bei Gasreaktionen erhöht erhöhter Druck die effektive Konzentration und fördert die Reaktion.
- Katalysatoren: Stoffe, die die Reaktion beschleunigen, ohne dabei dauerhaft verbraucht zu werden — z. B. Enzyme in Lebewesen.
- Licht: Manche Reaktionen sind photochemisch und benötigen Licht als Energiequelle.
Exotherme und endotherme Reaktionen
Bei exothermen Reaktionen wird Energie an die Umgebung abgegeben, meist in Form von Wärme (man spürt eine Erwärmung). Beispiele sind Verbrennungsvorgänge (dazu gehören Dinge, die brennen oder explodieren), und viele neutralisierende Reaktionen. Bei endothermenReaktionen wird Energie aus der Umgebung aufgenommen, wodurch die Umgebung abkühlt — ein bekanntes Beispiel ist die Fotosynthese, die Lichtenergie benötigt, um aus Kohlendioxid und Wasser Glucose zu bilden.
Der Übergangszustand einer Reaktion erfordert oft eine Anfangsenergie, die sogenannte Aktivierungsenergie. Selbst exotherme Reaktionen benötigen meist eine Aktivierungsenergie, bevor sie Energie netto freisetzen (z. B. muss Holz zuerst erhitzt werden, bevor es mit Luft reagiert und brennt).
Katalysatoren und Enzyme
Katalysatoren senken die Aktivierungsenergie und erhöhen so die Reaktionsgeschwindigkeit, ohne dauerhaft verbraucht zu werden. In biologischen Systemen übernehmen Enzyme diese Funktion; sie sorgen dafür, dass lebenswichtige Reaktionen bei niedrigen Temperaturen und unter milden Bedingungen schnell genug ablaufen.
Reversible Reaktionen und Gleichgewicht
Viele chemische Reaktionen sind reversibel — das heißt, Produkte können wieder zu Edukten reagieren. Wenn sich die Hin- und Rückreaktion im gleichen Tempo abspielen, spricht man von einem dynamischen Gleichgewicht. Veränderungen von Temperatur, Druck oder Konzentration können das Gleichgewicht verschieben (Le-Chatelier-Prinzip).
Typen chemischer Reaktionen
- Redox-Reaktionen (Elektronenübertragung): z. B. Verbrennung, Korrosion (Rosten).
- Säure-Base-Reaktionen (Protonenübertragung): z. B. Neutralisation von Säuren durch Basen.
- Fällungsreaktionen: Bildung eines unlöslichen Feststoffs in einer Lösung.
- Synthese- und Zersetzungsreaktionen: Aufbau bzw. Zerfall komplexerer Verbindungen.
- Polymerisation: Bildung langer Kettenmoleküle (Kunststoffe).
- Elektrochemische Reaktionen: siehe elektrochemische Reaktionen, z. B. in Batterien.
Chemie im Alltag und in der Technik
Chemische Reaktionen finden überall statt: in der Verbrennung und beim Kochen, in der Industrie bei der Herstellung von Kunststoffen oder Arzneimitteln, in Batterien beim Laden/Entladen und in den Zellen aller Lebewesen (Stoffwechselreaktionen). Die Kontrolle von Reaktionsbedingungen ist entscheidend für Ausbeute, Sicherheit und Effizienz.
Wichtig: Kernreaktionen sind anders
Kernreaktionen sind keine chemischen Reaktionen. An chemischen Reaktionen sind nur die Elektronen der Atome beteiligt; an Kernreaktionen sind die Protonen und Neutronen in den Atomkernen beteiligt. Kernreaktionen (z. B. radioaktiver Zerfall, Kernspaltung, Kernfusion) verändern die Identität der Elemente und setzen typischerweise viel größere Energiemengen frei als chemische Reaktionen.
Zusammengefasst: Chemische Reaktionen bedeuten das Umordnen von Atomen durch Brechen und Bilden von Bindungen. Sie folgen festen Gesetzen (z. B. Massenerhaltung), werden durch äußere Bedingungen und Katalysatoren beeinflusst und sind Grundlage zahlreicher natürlicher und technischer Prozesse.