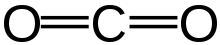Kohlendioxid (CO2) ist eine chemische Verbindung. Bei Raumtemperatur ist es ein Gas. Es besteht aus einem Kohlenstoff- und zwei Sauerstoffatomen. Menschen und Tiere setzen Kohlendioxid frei, wenn sie ausatmen. Auch jedes Mal, wenn etwas Organisches verbrannt wird (oder ein Feuer gemacht wird), entsteht Kohlendioxid. Pflanzen verwenden Kohlendioxid zur Herstellung von Lebensmitteln. Dieser Prozess wird Photosynthese genannt. Die Eigenschaften von Kohlendioxid wurden in den 1750er Jahren von dem schottischen Wissenschaftler Joseph Black untersucht.
Kohlendioxid ist ein Treibhausgas. Treibhausgase fangen Wärmeenergie ein. Treibhausgase verändern das Klima und das Wetter auf unserem Planeten, der Erde. Das nennt man Klimawandel. Treibhausgase sind eine Ursache für die globale Erwärmung, den Anstieg der Oberflächentemperatur der Erde.
Physikalisch-chemische Eigenschaften
Kohlendioxid ist farb- und geruchlos. Molare Masse: etwa 44 g/mol. In Wasser löst sich CO2 teilweise und bildet dabei Kohlensäure (H2CO3), wodurch Wasser leicht sauer wird. Bei tiefen Temperaturen geht CO2 direkt vom festen in den gasförmigen Zustand über (Sublimation); festes CO2 ist als Trockeneis bekannt und sublimiert bei −78,5 °C.
Vorkommen und Kreislauf
CO2 ist ein natürlicher Bestandteil der Atmosphäre und Teil des globalen Kohlenstoffkreislaufs. Es entsteht und wird aufgenommen durch Prozesse wie:
- Atmung von Pflanzen, Tieren und Menschen
- Zersetzung organischer Stoffe
- Vulkanische Aktivität
- Photosynthese (Pflanzen, Algen und einige Bakterien nehmen CO2 auf)
- Aufnahme durch Ozeane (Lösung und biologische Prozesse)
Anthropogene Quellen und Senken
Seit der Industrialisierung nimmt die Konzentration von Kohlendioxid in der Atmosphäre durch menschliche Aktivitäten stark zu. Wichtige Quellen sind:
- Verbrennung fossiler Brennstoffe (Kohle, Öl, Gas) für Energie und Verkehr
- Industrielle Prozesse, z. B. Zementherstellung
- Abholzung und Landnutzungsänderungen
- Bestimmte landwirtschaftliche Praktiken
Gleichzeitig wirken natürliche und gezielte Senken: Ozeane, terrestrische Vegetation (Wälder, Böden) und technische Verfahren wie Carbon Capture and Storage (CCS) oder Aufforstung können CO2 aus der Atmosphäre entfernen.
Klimawirkung und Folgen
CO2 ist das wichtigste vom Menschen beeinflusste Treibhausgas in Bezug auf den Beitrag zur langfristigen Erwärmung. Es absorbiert und emittiert Infrarotstrahlung, erhöht somit die Wärme (Strahlungsantrieb) in der Erdatmosphäre und trägt so zum Klimawandel bei. Wichtige Folgen sind:
- Erhöhung der globalen Durchschnittstemperatur
- Veränderungen von Niederschlagsmustern und regionalem Wetter
- Schmelzen von Gletschern und polarem Eis, Meeresspiegelanstieg
- Ozeanversauerung durch steigende CO2-Aufnahme, was Meeresökosysteme und kalkbildende Organismen belastet
Atmosphärische Konzentration und Verweildauer
Vor der Industrialisierung lag der CO2-Gehalt der Atmosphäre bei etwa 280 ppm (Teile pro Million). In den letzten Jahrzehnten stieg der Wert stark an und liegt heute bei über 420 ppm (Stand Anfang der 2020er Jahre). Ein Teil des vom Menschen emittierten CO2 wird innerhalb von Jahren bis Jahrzehnten von Ozeanen und Pflanzen aufgenommen; ein erheblicher Anteil verbleibt jedoch für Jahrhunderte bis Jahrtausende in der Atmosphäre, sodass historische Emissionen das Klima lange beeinflussen.
Messung und Überwachung
CO2-Konzentrationen werden weltweit an Messstationen (z. B. Mauna Loa) und per Satellit überwacht. Diese Daten zeigen langfristige Trends sowie saisonale Schwankungen durch Pflanzenwachstum.
Maßnahmen zur Reduktion
Zur Begrenzung der Erwärmung sind Maßnahmen nötig, die Emissionen verringern und CO2 aktiv entfernen:
- Umstellung auf erneuerbare Energien und Steigerung der Energieeffizienz
- Verkehrs- und Mobilitätswandel (Elektromobilität, öffentliche Verkehrsmittel, weniger private Pkw)
- Wiederaufforstung, Schutz bestehender Wälder und nachhaltige Landnutzung
- Entwicklung und Einsatz von CO2-Abscheidung und -Speicherung (CCS) sowie Technologien zur CO2-Entnahme aus der Atmosphäre
- Förderung klimafreundlicher Wirtschaftsweisen und Verhaltensänderungen
Zusammenfassung
Kohlendioxid ist ein natürliches Gas mit wichtigen Rollen im Leben auf der Erde (z. B. Photosynthese), aber seine übermäßige Freisetzung durch menschliche Aktivitäten treibt den Klimawandel voran. Neben der Erwärmung verursacht höheres CO2 auch Ozeanversauerung und weitere ökologische Folgen. Die Reduktion von CO2-Emissionen und die Verstärkung von Senken sind zentrale Bausteine, um ernsthafte Folgen für Klima, Umwelt und Gesellschaft zu begrenzen.