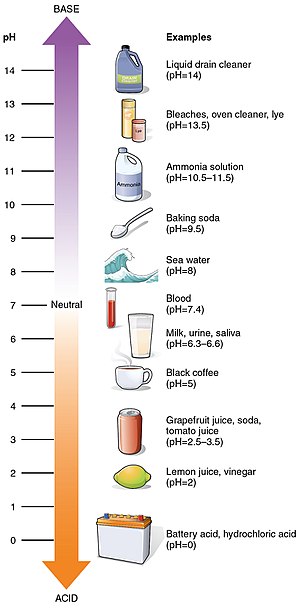
Der pH-Wert ist eine Skala zur Beschreibung der Azidität bzw. Basizität einer wässrigen Lösung. Sie reicht typischerweise von 0 bis 14 und gibt an, wie sauer oder alkalisch eine Substanz ist: je saurer eine Lösung, desto niedriger der pH‑Wert; je basischer/alkalischer, desto höher. Substanzen, die weder sauer noch alkalisch sind (also neutrale Lösungen), haben bei 25 °C normalerweise einen pH‑Wert von etwa 7. Säuren haben pH‑Werte kleiner als 7, Alkalien bzw. Basen Werte größer als 7.
Definition und mathematische Darstellung
Der pH‑Wert ist ein Maß für die Konzentration an Protonen (H+) in einer Lösung. Das Konzept wurde 1909 von S.P.L. Sørensen eingeführt. Das „p“ steht dabei für die deutsche Bezeichnung Potenz (im Sinne von Potenz oder Exponent), das „H“ für das Wasserstoffion (H+ bzw. das Hydroniumion H3O+).
Die in der einführenden Chemie am häufigsten verwendete Formel lautet
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{{{10}\links[{\mbox{H}}^{+}\rechts]}}
[H+] gibt die Konzentration der H+‑Ionen an (häufig wird auch [H3O+] benutzt), gemessen in Mol pro Liter (Molarität).
Die strengere (thermodynamische) Definition verwendet die Aktivität aH+ der Protonen:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{{10}\links[a_{\mathrm {H^{+}} }\rechts]}}
Die Aktivität aH+ berücksichtigt Wechselwirkungen zwischen Ionen und kann von der nominellen Konzentration abweichen; für verdünnte Lösungen liefert die Konzentration jedoch meist nahezu denselben pH‑Wert wie die Aktivität. Der pH‑Wert selbst ist dimensionslos (kein physikalisches Einheitensymbol).
Zusammenhang mit Hydroxidionen und pOH
In wässrigen Lösungen stehen Wasserstoff‑ und Hydroxidionen in Beziehung über das Ionenprodukt des Wassers Kw:
- [H+] · [OH−] = Kw
- pKw = pH + pOH
Bei 25 °C gilt Kw ≈ 1·10^−14 mol^2·L^−2, daher pKw ≈ 14; dadurch ergibt sich oft die vertraute Beziehung pH + pOH = 14 (Temperaturabhängig — bei anderen Temperaturen weicht pKw ab).
Der pOH wird analog definiert als pOH = −log10[OH−].
Messung des pH‑Wertes
Gängige Messmethoden:
- pH‑Elektroden (pH‑Meter): Glas‑Sonde misst das elektrochemische Potential; Ergebnis ist schnell und genau. Regelmäßige Kalibrierung mit Standardpufferlösungen (z. B. pH 4, 7, 10) und Pflege der Elektrode sind wichtig.
- Indikatorpapier / Universalindikator: Schnelle, einfache Abschätzung durch Farbvergleich; für genaue Messungen weniger geeignet.
- pH‑Indikatoren: Substanzen wie Phenolphthalein, Methylorange, die bei bestimmten pH‑Bereichen ihre Farbe ändern; in Titrationen weit verbreitet.
- Titration: Chemische Bestimmung durch Neutralisation mit bekannter Maßlösung; liefert genaue Werte für Säure-/Basenkonzentration und pKa‑Werte.
Bedeutung und Anwendungen
Der pH‑Wert ist in vielen Bereichen entscheidend:
- Biologie und Medizin: Viele Enzyme und physiologische Prozesse sind pH‑abhängig. Blut hat z. B. einen engen Normalbereich von etwa 7,35–7,45; Abweichungen können lebensbedrohlich sein.
- Umwelt: pH beeinflusst die Löslichkeit von Nährstoffen und Schadstoffen. Regenwasser ist leicht sauer (typisch um pH 5,6 ohne Luftverschmutzung), saurer Regen kann Ökosysteme schädigen.
- Lebensmittel und Haushalt: Haltbarkeit, Geschmack und mikrobielles Wachstum hängen vom pH ab (z. B. Essig pH ~2–3, Milchprodukte pH ≈4–6).
- Industrie: Galvanik, chemische Synthesen, Abwasserbehandlung, Landwirtschaft — überall muss der pH kontrolliert werden.
- Laborpraxis: Viele Reaktionen erfordern einen definierten pH‑Wert (z. B. Pufferlösungen in der Biochemie).
Puffer und Stabilisierung des pH
Puffer sind Lösungen, die den pH bei Zugabe von Säure oder Base nur wenig ändern, üblicherweise bestehen sie aus einem schwachen Säure/Basen‑Paar (z. B. Essigsäure/Acetat). Puffer sind zentral in biologischen Systemen (z. B. Bicarbonat‑Puffersystem im Blut) und technischen Prozessen.
Typische pH‑Werte (Beispiele)
- starke Batteriesäure (Schwefelsäure, konzentriert): pH < 0
- Magensäure: ca. 1–2
- Zitronensaft: ca. 2
- Essig: ca. 2–3
- Regenwasser (unverschmutzt): ca. 5,6
- reines Wasser (25 °C): pH ≈ 7
- Blut: ca. 7,35–7,45
- Meerwasser: ca. 8,1
- Seifenlösungen/Ammoniak: ca. 10–12
- Natronlauge (stark basisch): pH ≈ 14
Extremwerte, Temperaturabhängigkeit und Sicherheit
Obwohl die Skala von 0–14 gebräuchlich ist, sind auch Werte < 0 oder > 14 möglich (sehr starke Säuren bzw. Laugen bzw. hochkonzentrierte Lösungen). Der neutrale pH‑Wert von 7 bezieht sich auf 25 °C; mit steigender oder sinkender Temperatur ändert sich Kw und damit der pH einer neutralen Lösung.
Stark saure oder basische Lösungen sind korrosiv und gefährlich — geeignete Schutzmaßnahmen (Schutzbrille, Handschuhe, Abzug) sind Pflicht.
Zusammenfassung
Der pH‑Wert ist ein zentrales, dimensionsloses Maß für die Azidität einer Lösung, definiert als der negative dekadische Logarithmus der Protonenaktivität (praktisch oft der Konzentration). Er beeinflusst chemische Reaktionen, biologische Prozesse und industrielle Anwendungen und wird mit pH‑Metern, Indikatoren oder durch Titration bestimmt. Pufferlösungen stabilisieren den pH‑Wert und verhindern schädliche Schwankungen.
Alkalische Substanzen haben anstelle von Wasserstoffionen eine erhöhte Konzentration von Hydroxidionen (OH−).
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)