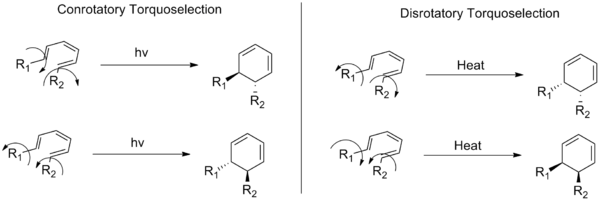
Diese Begriffe beschreiben zwei Klassen einer elektrozyklischen Reaktion (eine Art von organisch-chemischen Reaktionen). In einem rotatorischen Modus bewegen sich die Substituenten, die sich an den Enden eines konjugierten Doppelbindungssystems befinden, während der Ringöffnung oder des Ringschlusses in die gleiche Richtung (im oder gegen den Uhrzeigersinn). In einem disrotatorischen Modus bewegen sie sich in entgegengesetzte Richtungen.
Ein Beispiel ist die Umwandlung von trans-cis-trans-2,4,6-Octatrien in cis-Dimethylcyclohexadien (oben in der Abbildung). Die Orbitalmechanik der Reaktion benötigt einen disrotatorischen Modus. Die Orbitalsymmetrie des höchsten besetzten Molekülorbitals (HOMO) des Octatriens erfordert, dass sich die End-pi-Orbitale in entgegengesetzte Richtungen bewegen, um die korrekte Symmetrie zu bilden, die in der Sigma-Bindung gefunden wurde.
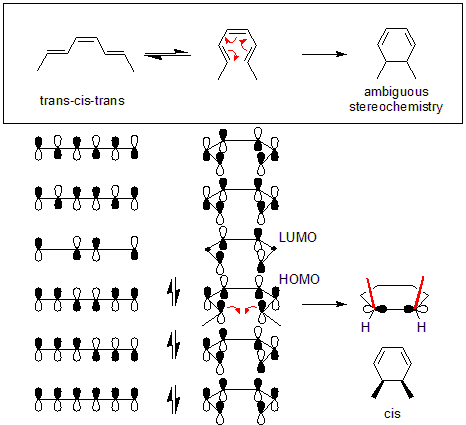
Thermische Umlagerungen aller konjugierten Systeme, die 4n + 2 pi-Elektronen enthalten, sind stereospezifisch. Dies beruht auf der Erhaltung der Bahnsymmetrie im höchsten besetzten Molekülorbital. Systeme, die 4n pi-Elektronen enthalten, zeigen den entgegengesetzten Rotationsmodus. Dies gilt auch für Umlagerungen von 4n + 2 pi (wobei n eine ganze Zahl ist) Elektronen, die durch Licht (photoinduziert) getrieben werden. Photoinduzierte Umlagerungen von 4n pi-Elektronensystemen (wobei die Anzahl der Elektronen durch 4 teilbar ist) folgen der disrotatorischen Regel.
Die Woodward-Hoffmann-Regeln fassen die oben genannten unterschiedlichen Reaktionen zusammen.
Das folgende Bild zeigt auch den Unterschied zwischen konrotatorischen und disrotatorischen Reaktionen: