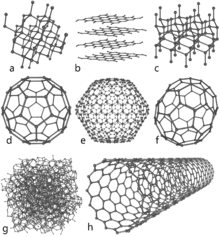
Es gibt mehrere Allotrope von Kohlenstoff. Diamant und Graphit sind die bekanntesten und am besten untersuchten Formen. Während Graphit elektrisch leitfähig ist und sich aufgrund seiner geschichteten Struktur als Schmiermittel eignet, ist Diamant extrem hart und optisch sehr brillant. Graphit wird zum Beispiel als Material in den Elektroden einer elektrischen Bogenlampe verwendet. Außerdem gilt Graphit als die stabilste Form von festem Kohlenstoff unter Normalbedingungen.
Was sind Allotrope?
Allotrope sind verschiedene Formen desselben chemischen Elements, die sich nur in der Anordnung und Bindung der Atome unterscheiden. Diese unterschiedlichen Bindungsmuster führen zu deutlich verschiedenen physikalischen und chemischen Eigenschaften. Bei Kohlenstoff sind die Unterschiede besonders ausgeprägt, weil das Kohlenstoffatom verschiedene Bindungstypen eingehen kann (z. B. sp2- und sp3-Hybridisierung). Neben kristallinen Formen spielen auch die Anordnung ganzer Moleküle oder Schichten eine Rolle bei der Bildung größerer Strukturen.
Graphit: Struktur, Eigenschaften und Anwendungen
Graphit besteht aus Schichten von sechseckigen Kohlenstoffringen, in denen die Atome durch sp2-Hybridisierung verbunden sind. Innerhalb der Ebene sind Elektronen delokalisiert, weshalb Graphit elektrische Leitfähigkeit in der Ebene zeigt. Zwischen den Schichten wirken nur schwache van-der-Waals-Kräfte, was die charakteristische Gleiteigenschaft erklärt – daher seine Verwendung als Schmiermittel und in Stiften (Bleistiftminen).
- Leitfähigkeit: Elektrische Leitfähigkeit vorwiegend in der Ebene (anisotrop).
- Mechanische Eigenschaften: Weich in Richtung der Schichten, spröde senkrecht dazu; gute Schichtbarkeit.
- Thermische Eigenschaften: Gute Wärmeleitfähigkeit entlang der Ebenen.
- Stabilität: Thermodynamisch die stabilste kristalline Form von festem Kohlenstoff bei Standardbedingungen.
- Anwendungen: Elektroden (Elektroden), Schmierstoffe, Bleistifte, hitzebeständige Werkstoffe, neutronenmoderierendes Material in Kernreaktoren, Leitschichten in Batterien und Elektrokontakten.
Diamant: Aufbau, Eigenschaften und Anwendungen
Diamant hat eine kubische Kristallstruktur, in der jedes Kohlenstoffatom sp3-hybridisiert und tetraedrisch an vier Nachbarn gebunden ist. Diese dreidimensionale, sehr starke Vernetzung ist der Grund für die außergewöhnliche Härte von Diamant. Er ist das härteste bekannte natürliche Mineral, was ihn zu einem sehr effektiven Schleifmittel und Schneidwerkstoff macht.
- Härte: Höchste Härte unter natürlichen Materialien (auf der Mohs-Skala 10); deshalb weit verbreitet in Schleif- und Schneidwerkzeugen.
- Optik: Hohe Lichtbrechung und Dispersion; deshalb geschätzt als Schmuckstück.
- Elektrische Eigenschaften: Reiner Diamant ist ein elektrischer Isolator, kann aber durch Dotierung (z. B. Bor) elektrisch leitend werden.
- Thermische Eigenschaften: Sehr hohe Wärmeleitfähigkeit (Diamanten leiten Wärme besser als die meisten anderen Nichtmetalle).
- Stabilität: Unter Normalbedingungen kinetisch sehr stabil, thermodynamisch jedoch gegenüber Graphit metastabil; Diamant kann bei sehr hohen Temperaturen und in Gegenwart von Sauerstoff zu Kohlenstoffoxid oxidiert werden.
- Anwendungen: Schmuck, Schneid- und Bohrwerkzeuge, Präzisionsoptik, Wärmeleiter in Hochleistungsanwendungen, elektronische Bauteile aus dotiertem Diamant und industrielle Abrasive.
Weitere Kohlenstoffallotrope
Neben Diamant und Graphit gibt es weitere wichtige Allotrope:
- Graphen: Eine einzelne Schicht aus dem Graphit-Gitter. Außergewöhnlich hohe elektrische und thermische Leitfähigkeit sowie enorme Festigkeit pro Gewicht.
- Fullerene (z. B. C60): Kugelförmige Moleküle aus Kohlenstoffringen, interessante Eigenschaften für Forschung und Materialwissenschaft.
- Kohlenstoff-Nanoröhren: Zylindrische Graphenrollen mit hoher Zugfestigkeit und Leitfähigkeit, relevant für Nanotechnologie und Verbundwerkstoffe.
- Amorpher Kohlenstoff, Ruß und Holzkohle: Unregelmäßig vernetzte Formen mit breitem Einsatzspektrum (Filtration, Aktivkohle, Beschichtungen).
Bildung, Synthese und thermodynamische Aspekte
Die Bildung der verschiedenen Allotrope hängt von Druck, Temperatur und Synthesebedingungen ab. Natürliche Diamanten entstehen tief in der Erdkruste oder im oberen Erdmantel bei sehr hohen Drücken und Temperaturen. Industriell werden Diamanten durch Hochdruck-Hochtemperatur-Verfahren (HPHT) oder durch chemische Gasphasenabscheidung (CVD) hergestellt.
Wichtig ist der Unterschied zwischen thermodynamischer Stabilität und kinetischer Stabilität: Unter Normalbedingungen ist Graphit die thermodynamisch stabilste Form, während Diamant kinetisch stabil ist und deshalb über geologische Zeiträume erhalten bleiben kann, obwohl er energetisch weniger günstig ist.
Zusammenfassung
Kohlenstoff zeigt durch seine Allotrope ein breites Spektrum an physikalischen Eigenschaften: von sehr weichen, leitfähigen Schichten im Graphit über das härteste natürliche Material Diamant bis hin zu hochmodernen Nanomaterialien wie Graphen und Kohlenstoff-Nanoröhren. Diese Vielfalt erklärt, warum Kohlenstoff in so vielen Bereichen der Technik, Industrie und Forschung eine zentrale Rolle spielt.