Fluoreszenz ist das Licht, das von bestimmten Substanzen abgegeben wird, wenn sie Licht oder andere elektromagnetische Strahlung absorbieren. Zuerst absorbiert der Stoff die Energie, dann strahlt er Licht aus. Wenn die Lichtquelle entfernt wird, tritt die Fluoreszenz nicht mehr auf. Es handelt sich um eine Form der Lumineszenz. Fluoreszenz ist damit ein unmittelbares Re-Emission‑Phänomen: die Anregung erfolgt durch Photonen, die Emission erfolgt typischerweise innerhalb von Billionstel bis Milliardstel Sekunden nach der Anregung.
Funktionsprinzip
Auf molekularer Ebene bedeutet Fluoreszenz, dass ein Elektron eines Moleküls durch absorbierte Energie (Photon) in einen angeregten Zustand gehoben wird. Nach schneller innerer Relaxation (vibrationsfreie Abkühlung) kehrt das Elektron in einen niedrigeren elektronischen Zustand zurück und gibt dabei ein Photon ab. Dieser Ablauf lässt sich schematisch im sogenannten Jablonski-Diagramm darstellen: Übergang vom Grundzustand S0 in den angeregten Singulettzustand S1 (oder höher), gefolgt von nichtstrahlenden Relaxationsprozessen und schließlich der strahlenden Rückkehr S1 → S0 (Fluoreszenz).
In den meisten Fällen hat das abgegebene Licht eine längere Wellenlänge und eine geringere Energie als das absorbierte Licht. Dieser Wellenlängenunterschied wird als Stokes-Verschiebung bezeichnet und ist wichtig, um Emissions- und Anregungslicht optisch zu trennen. Fluoreszenz findet in der Regel sehr schnell statt (Lebensdauern im Bereich von Pikosekunden bis Nanosekunden), im Gegensatz zur Phosphoreszenz, die durch langsame Übergänge über Triplettzustände deutlich längere Nachleuchtzeiten aufweist.
Wichtige Eigenschaften
- Stokes-Verschiebung: Differenz zwischen Anregungs- und Emissionsmaximum (in Nanometern).
- Quantenausbeute (Quantum Yield): Verhältnis der emittierten zu den absorbierten Photonen; wichtig für die Helligkeit eines Fluorophors.
- Lebensdauer (Lifetime): mittlere Zeit, die ein Molekül im angeregten Zustand verbleibt; wichtig für zeitaufgelöste Messungen.
- Photobleaching: irreversible Zerstörung des Fluorophors durch wiederholte Belichtung.
- Quenching: Verminderung der Fluoreszenz durch Sauerstoff, Ionen, pH‑Änderungen oder andere Moleküle.
- Empfindlichkeit gegenüber Umgebung: Lösungsmittel, Temperatur und pH beeinflussen Emissionsspektrum und Intensität (Solvatochromie).
Messung und Instrumente
Fluoreszenz wird mit speziellen Geräten gemessen, z. B. mit Fluoreszenzspektrometern (Spektrofluorometer), die Anregungs- und Emissionsspektren aufzeichnen. In der Mikroskopie werden Filter, Dichroische Spiegel und Laser eingesetzt, um Anregungs- und Emissionslicht zu trennen. Wichtige mikroskopische Techniken sind:
- Fluoreszenzmikroskopie (Widefield)
- Konfokale Laser-Scanning-Mikroskopie
- Zwei-Photonen-Mikroskopie (deep tissue imaging)
- TIRF (Total Internal Reflection Fluorescence) für Oberflächennahe Messungen
- Durchflusszytometrie (Flow Cytometry) für Zellanalyse
Bekannte Fluorophore und Markersysteme sind z. B. GFP (Grün fluoreszierendes Protein), FITC, Rhodamin, Alexa‑Farbstoffe u. a. Für quantitative Messungen sind Kalibrierung, geeignete Filter und Korrektur auf Instrumentenantwort wichtig.
Anwendungen
Fluoreszenz wird in vielen Bereichen eingesetzt:
- Mineralogie und Gemmologie: Bestimmung von Mineralen und Effekten in Edelsteinen.
- Chemische Sensoren (Fluoreszenzspektroskopie): Erkennung von Ionen, Gasen oder organischen Verbindungen durch Fluoreszenzänderungen.
- Farbstoffe und Leuchtstoffe: Herstellung von Markern, Textil- und Sicherheitsdruckfarben.
- Biologische Detektion: Fluoreszenzmarkierte Antikörper in der Immunfluoreszenz, Fluoreszenz-in-situ‑Hybridisierung (FISH) oder markierte Nucleinsäuren.
- Fluoreszenzlicht und Beleuchtungstechnik: spezielle Leuchtmittel und Sicherheitsmarkierungen.
- Medizinische Diagnostik: Bildgebung, Nachweis von Biomarkern, Endoskopische Verfahren.
- Forensik: Spurennachweis (z. B. Körperflüssigkeiten unter UV), Dokumentenprüfung.
- Umweltanalytik: Nachweis von Schadstoffen, Algenblüten oder Ölverschmutzung.
- FRET (Förster-Resonanz-Energie-Transfer): Untersuchung von Protein‑Protein‑Interaktionen auf Nanometer‑Skala.
- Single-Molecule‑Techniken und DNA-Sequenzierung: ultrasensible Analyse von einzelnen Molekülen.
Fluoreszenz in den Biowissenschaften
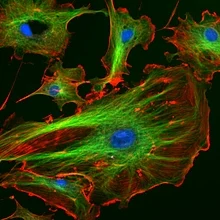
Die Fluoreszenz in den Biowissenschaften ist eine Möglichkeit, biologische Moleküle zu verfolgen. An ein Protein oder eine andere Komponente kann ein Fluoreszenzfarbstoff gebunden sein, der es einem Wissenschaftler ermöglicht, das spezifische Protein mit einem Mikroskop visuell zu finden. Typische Methoden sind:
- Gentragende Fluoreszenzproteine (z. B. GFP‑Fusionsproteine) zur Darstellung von Lokalisierung und Dynamik in lebenden Zellen.
- Immunfluoreszenz mit fluoreszenzmarkierten Antikörpern zur gezielten Detektion von Proteinen in Fixaten.
- Lebendzell‑Markierung mit Zellpermeablen Dyes, organellspezifischen Markern oder pH‑sensitiven Fluorophoren.
Bei biologischen Experimenten sind Phototoxizität, Photobleaching und die richtige Wahl von Farbstoffen und Filterkombinationen entscheidend für verlässliche Ergebnisse.
Praktische Hinweise und Sicherheit
- Sicherheit: Ultraviolettes Licht (z. B. zur Anregung) kann schädlich für Augen und Haut sein — geeigneten Augenschutz und Abschirmung verwenden.
- Photobleaching reduzieren: geringere Belichtungszeiten, Antifade‑Reagenzien und empfindlichere Detektoren verwenden.
- Messbedingungen standardisieren: pH, Temperatur und Lösungsmittel beeinflussen Fluoreszenz; für Vergleiche konsistente Bedingungen wählen.
- Interferenzen vermeiden: Autofluoreszenz von Proben oder Materialien kann die Messung stören — geeignete Kontrollen einplanen.
Fluoreszenz ist somit ein vielseitiges, empfindliches und schnell reagierendes Werkzeug in Forschung, Industrie und Technik. Mit dem richtigen Verständnis der physikalischen Grundlagen und der praktischen Einschränkungen lassen sich präzise und aussagekräftige Analysen durchführen.