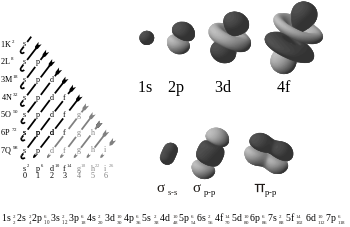
In der Chemie sind pi-Bindungen (π-Bindungen) kovalente chemische Bindungen, bei denen sich die Bahn eines Elektrons mit der Bahn eines anderen kreuzen (überlappen). Die Elektronen haben eine lappenförmige Achterbahn (siehe Bild). Es gibt zwei Überlappungsbereiche, da sich die Bahnen auf beiden Lappen überlappen. Nur eine der Knotenebenen des Orbitals verläuft durch beide beteiligten Kerne.
Der griechische Buchstabe π in ihrem Namen bezieht sich auf p-Orbitale. Die Orbitalsymmetrie der pi-Bindung sieht auf der Bindungsachse gesehen gleich aus wie das p-Orbital. Die p-Orbitale haben normalerweise diese Art der Bindung. Bei den D-Orbitalen wird ebenfalls angenommen, dass sie eine pi-Bindung verwenden, aber das ist nicht unbedingt das, was in Wirklichkeit geschieht. Die Idee der Bindung von d-Orbitalen passt zu der Theorie der Hypervalenz.
Pi-Anleihen sind in der Regel schwächer als Sigma-Anleihen. Die Quantenmechanik sagt, dass dies darauf zurückzuführen ist, dass die Orbitalbahnen parallel sind, so dass es viel weniger Überlappungen zwischen den p-Orbitalen gibt.
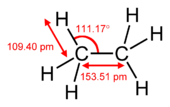
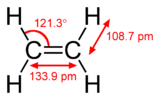
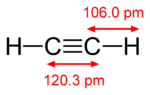
Pi-Bindungen entstehen, wenn zwei Atomorbitale durch zwei Überlappungsbereiche in Kontakt sind. Pi-Bindungen sind stärker gestreute Bindungen als die Sigma-Bindungen. Elektronen in pi-Bindungen werden manchmal als pi-Elektronen bezeichnet. Molekülfragmente, die durch eine pi-Bindung verbunden sind, können sich nicht um diese Bindung drehen, ohne die pi-Bindung zu brechen. Durch die Rotation werden die parallelen Bahnen der beiden p-Orbitale zerstört.