Kovalente Bindungen sind chemische Bindungen zwischen zwei Nichtmetallatomen. Ein Beispiel ist Wasser, bei dem sich Wasserstoff (H) und Sauerstoff (O) zu (H2O) verbinden. Eine volle äußere Schale hat normalerweise acht Elektronen, oder zwei im Falle von Wasserstoff oder Helium. Valenzelektronen sind die Elektronen, die vergleichsweise locker in der äußeren Schale des Atoms gehalten werden. Die Struktur von Elektronenschalen wird durch die Quantenmechanik bestimmt).
Die Anzahl der Elektronen in einem Atom wird durch die Anzahl der Protonen in dem Atom bestimmt. Elektronen umkreisen Atomkerne, und sie sind wie unscharfe Umlaufbahnen um einen Atomkern. Die erste Schicht hat bis zu zwei Elektronen. Die Schichten danach enthalten in der Regel bis zu acht. Kovalente Bindungen werden durch Atome gebildet, die sich Valenzelektronen teilen.
Hatte ein Atom beispielsweise neun Elektronen, so kreisen die ersten beiden auf einer Bahn sehr nahe am Kern, die nächsten sieben auf einer etwas weiter entfernten. Die äußeren sieben Elektronen werden weniger fest gehalten als die inneren zwei Elektronen, weil sie weiter vom positiv geladenen Kern entfernt sind. Wenn sich dieses Atom einem anderen Atom mit einem lose gehaltenen Elektron in seiner äußeren Schale nähert, wird ein neues Orbital für das lose gehaltene Elektron verfügbar. Dieses neue Elektronenorbitale ist an beide Atomkerne gebunden und hat ein niedrigeres Energieniveau als das ursprüngliche Elektronenorbitale. Das Elektron kann spontan dorthin springen und mit der überschüssigen Energie ein Photon aussenden. Jetzt haben wir ein Elektron, das beide Atome umkreist, was dazu führt, dass das Atom, das das Elektron geliefert hat, eine kleine positive Nettoladung und das andere Atom eine kleine negative Nettoladung hat. Die beiden Atome werden nun durch die elektromagnetische Anziehungskraft zwischen positiven und negativen Ladungen zusammengehalten. Dies nennt man eine kovalente Bindung. Um diese Bindung aufzubrechen, wird die gleiche Energiemenge benötigt, die bei ihrer Bildung freigesetzt wurde.
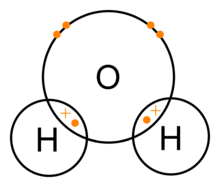
Ein Wassermolekül besteht aus einem Sauerstoffatom und zwei Wasserstoffatomen, die durch eine kovalente Bindung zusammengehalten werden. In diesem Fall teilt sich das Sauerstoffatom mit jedem Wasserstoffatom ein Elektron. Dies bedeutet, dass die Sauerstoffatome eine kleine positive Nettoladung und das Wasserstoffatom eine kleine negative Nettoladung hat. Infolgedessen werden die Sauerstoff- und Wasserstoffatome durch die elektromagnetische Kraft voneinander angezogen. Aus diesem Grund ist das Wassermolekül ein polares Molekül: seine Ladung ist nicht gleichmäßig verteilt.