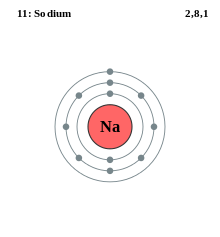
Eine Elektronenhülle ist der äußere Teil eines Atoms um den Atomkern herum. Sie befindet sich dort, wo sich die Elektronen befinden, und ist eine Gruppe von Atomorbitalen mit dem gleichen Wert der Hauptquantenzahl n.
Elektronenschalen haben eine oder mehrere Elektronen-Unterschalen, oder Unterebenen. Diese Unterebenen haben zwei oder mehr Orbitale mit der gleichen Drehimpuls-Quantenzahl l. Elektronenschalen bilden die Elektronenkonfiguration eines Atoms. Die Anzahl der Elektronen, die sich in einer Schale befinden können, ist gleich 2 n 2 {\Anzeigeart 2n^{2}}}. 
Der Name für Elektronenschalen stammt vom Bohr'schen Modell, bei dem man glaubte, dass Gruppen von Elektronen den Kern in bestimmten Abständen umkreisen, so dass ihre Bahnen "Schalen" bilden. Dieser Begriff wurde von dem dänischen Arzt Niels Henrik David Bohr vorgestellt.