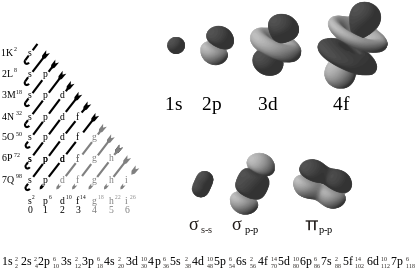
Atomorbitale sind die den Atomkern umgebenden Orte, an denen sich die Elektronen mit größter Wahrscheinlichkeit zu einem bestimmten Zeitpunkt befinden. Es handelt sich um eine mathematische Funktion, die das wellenartige Verhalten entweder eines Elektrons oder eines Elektronenpaares in einem Atom beschreibt.
Das Wort "Orbital" wird verwendet, weil man annahm, dass sich die Elektronen ähnlich wie im Sonnensystem verhalten, in dem der Kern wie die Sonne ist und die Elektronen wie die Planeten kreisen.
Die Anzahl der Atomorbitale in einem Element wird durch die Periode definiert, in der sich das Element befindet. Elektronen bewegen sich zwischen den Orbitalen, je nachdem, wie schnell sie sich bewegen und wie viele andere Elektronen vorhanden sind.
In der Atomtheorie und Quantenmechanik ist ein Atomorbital eine Quantenzahl. Jedes dieser Orbital kann mit einem oder zwei Elektronen besetzt sein. Die Art und Weise, wie die Orbitale angeordnet sind, hängt mit den Elektronenkonfigurationen der Atome zusammen. Sie wurden aus Beschreibungen früherer Spektroskopiker von bestimmten Alkalimetall-Spektroskopielinien als scharf, prinzipiell, diffus und fundamental abgeleitet.