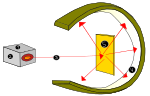
Im Jahr 1850 konstruierte Sir William Crookes eine "Entladungsröhre", d.h. eine Glasröhre, bei der die Luft entfernt wird und an deren Enden metallische Elektroden an eine Hochspannungsquelle angeschlossen sind. Beim Erzeugen eines Vakuums in der Röhre ist eine Lichtentladung zu sehen, die von der Kathode (negativ geladene Elektrode) zur Anode (positiv geladene Elektrode) verläuft. Crookes nannten die Emission "Kathodenstrahlen".
Nach den Kathodenstrahl-Experimenten stellte Sir Joseph John Thomson fest, dass der emittierte Strahl durch negative Ladungen gebildet wurde, weil sie vom positiven Pol angezogen wurden. Thomson wusste, dass die Atome elektrisch neutral waren, aber er stellte fest, dass ein Atom die gleiche Menge negativer und positiver Ladungen haben musste, damit dies geschehen konnte. Die negativen Ladungen wurden Elektronen (e-) genannt.
Entsprechend den über die neutrale Ladung der Atome aufgestellten Annahmen schlug Thomson das erste Atommodell vor, das als positiv geladene Kugel beschrieben wurde, in die die Elektronen (mit negativen Ladungen) eingelagert waren. Es ist als das Pflaumenpuddingmodell bekannt.
Im Jahr 1906 stellte Robert Millikan fest, dass die Elektronen eine Coulomb (C)-Ladung von -1,6 * 10-19 hatten, was die Berechnung ihrer Masse als winzig klein, gleich 9,109 * 10-31 kg, erlaubte.
Gleichzeitig konnte Eugene Goldstein 1886 durch Experimente mit Kathodenentladungsröhren feststellen, dass die positiven Ladungen eine Masse von 1,6726 * 10-27 kg und eine elektrische Ladung von +1,6 * 10 -19 C hatten. Lord Ernest Rutherford nannte diese positiv geladenen Teilchen später Protonen