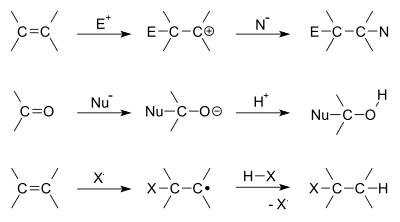
In der organischen Chemie findet eine Additionsreaktion statt, wenn zwei Moleküle zusammenkommen, um ein größeres Molekül zu bilden. Dies kann nur geschehen, wenn eines der Moleküle bereits eine Doppel- oder Dreifachbindung aufweist. Dies können Kohlenstoff–Kohlenstoff-Bindungen oder sogar Kohlenstoff–Sauerstoff, Kohlenstoff–Stickstoff und andere sein. Eines der beiden Moleküle wird als Nukleophil bezeichnet, und dies ist dasjenige, das die Elektronen an das andere Molekül abgibt, um die neue Bindung herzustellen. Das andere Molekül wird als Elektrophil bezeichnet, und dies ist dasjenige, das die Elektronen erhält.
Eine Additionsreaktion ist das Gegenteil einer Eliminationsreaktion. Gängige Beispiele für Additionsreaktionen sind die Addition von Wasser über eine Doppelbindung und der nukleophile Angriff auf ein Carbonyl.
Arten von Additionsreaktionen
- Elektrophile Addition: Typisch für Alkene und Alkine. Ein Elektrophil greift die π-Bindung an, es entsteht oft ein positiviertes Zwischenprodukt (z. B. Carbokation) und anschließend erfolgt der Angriff eines Nukleophils. Beispiele: Halogenierung, Hydratisierung (säurekatalysierte Wasseraddition), Addition von HX.
- Nukleophile Addition: Besonders bei polaren Mehrfachbindungen wie Carbonylgruppen (C=O). Ein Nukleophil greift das elektrisch positive Kohlenstoffatom an, es entstehen Imin-, Alkohole oder Additionsprodukte (z. B. Grignard-Reagenzien an Aldehyde/Ketone).
- Radikalische Addition: Verläuft über Radikalzwischenstufen, z. B. die anti‑Markovnikov-Addition von HBr in Gegenwart von Peroxiden oder radikalische Polymerisation von Alkenen.
- Perizyklische / Concerted Additionen: Reaktionen ohne isolierbare Zwischenstufen, z. B. die Diels–Alder-Reaktion (Cycloaddition), die simultan mehrere Bindungen bildet.
- Konjugierte Addition (1,4‑Addition, Michael‑Addition): Nukleophile Additionen an α,β‑ungesättigte Carbonylverbindungen, bei denen das Nukleophil das β‑Kohlenstoffatom angreift und ein stabilisiertes Enolat bildet.
Mechanismen und wichtige Konzepte
- Regioselektivität (Markovnikov vs. anti‑Markovnikov): Bei unsymmetrischen Alkenen entscheidet die Stabilität des Zwischenprodukts (z. B. Carbokation). Nach der Markovnikov‑Regel addiert sich das Wasserstoffatom dort, wo bereits mehr Wasserstoff sitzt; anti‑Markovnikov‑Addition (z. B. bei HBr mit Peroxiden) läuft über Radikale und liefert das entgegengesetzte Produkt.
- Stereochemie (syn vs. anti): Manche Additionen finden syn (beide Substituenten von derselben Seite) statt, z. B. katalytische Hydrogenierung (H2/Pt), andere anti (entgegengesetzte Seiten), z. B. Halogenierung mit Br2 (über Bromonium‑Ion). Die Stereochemie beeinflusst die Konfiguration der neu gebildeten stereogenen Zentren.
- Zwischenstufen und Umlagerungen: Bei elektrophilen Additionen können Carbokationen entstehen, die ggf. Umlagerungen (Hydrid- oder Alkylshift) zeigen, um stabilere Kationen zu bilden—dies beeinflusst Produktverteilung.
- Reversibilität: Viele Additionen sind unter bestimmten Bedingungen reversibel; die Gegenreaktion ist eine Eliminierung. Sensible Additionsprodukte (z. B. Halogenhydrine) können leicht wieder reagieren.
Beispiele aus der Praxis
- Hydratisierung von Alkenen (säurekatalysiert): Addition von Wasser an eine C=C‑Doppelbindung zu Alkoholen (Markovnikov‑Produkt bei Säurekatalyse).
- Hydroboration‑Oxidation: Syn‑Addition von BH3 an ein Alken, gefolgt von Oxidation zu einem Alkohol; liefert anti‑Markovnikov‑Produkte.
- Halogenaddition (Br2, Cl2): Anti‑Addition über ein Bromonium-/Chloronium‑Ion; typisch ist die Bildung von vicinalen Dihalogeniden.
- Hydrierung (H2 mit Übergangsmetallkatalysator): Syn‑Addition von Wasserstoff an Alkene/Alkine zur gesättigten Verbindung (z. B. Ethin → Ethan).
- Nukleophile Addition an Carbonylverbindungen:
- Grignard‑Reagenzien addieren an Aldehyde/Ketone und liefern nach Hydrolyse Alkohole.
- Reduktion mit NaBH4 oder LiAlH4 (Hydrid‑Transfer) liefert Alkohole.
- Bildung von Hemiacetalen/Acetalen bei Addition von Alkoholen an Carbonyle (sauer katalysiert).
- Michael‑Addition: Konjugierte Addition von Enolaten oder anderen Nucleophilen an α,β‑ungesättigte Carbonylsysteme (wichtig in der organischen Synthese).
- Diels–Alder‑Reaktion: [4+2]-Cycloaddition zwischen Dienen und Dienophilen; eine pericyclische, konzertierte Additionsreaktion zur Bildung cyclischer Systeme.
- Polymerisation: Ketten‑Additionspolymerisation (z. B. Bildung von Polyethylen) verknüpft viele Monomere über sukzessive Additionen an reaktive Endradikale oder Kationen.
Faktoren, die die Additionsreaktion beeinflussen
- Substituenten am Mehrfachbindungspartner: Elektronenziehende oder -schiebende Gruppen verändern Elektronendichte und Stabilität von Zwischenstufen (z. B. Carbokationen).
- Solvens und Katalysatoren: Protische vs. aprotische Lösungsmittel, Säuren, Basen oder Metallkatalysatoren ändern Mechanismus, Geschwindigkeit und Selektivität.
- Temperatur und Druck: Beeinflussen Reaktionsgeschwindigkeit und Gleichgewicht; manche Additionen (z. B. Diels–Alder) sind temperaturabhängig.
- Sterische Effekte: Großräumige Substituenten können den Zugang zum Reaktionszentrum behindern und die stereochemische Einstellung beeinflussen.
Zusammenfassung
Additionsreaktionen sind grundlegende Umwandlungen in der organischen Chemie, bei denen an einer vorhandenen Mehrfachbindung zwei Atome oder Gruppen ergänzt werden. Sie kommen in vielen Varianten vor (elektrophil, nukleophil, radikalisch, concerted) und sind zentral für die Synthese von Alkoholen, Halogenverbindungen, cyclischen Strukturen und Polymeren. Wichtige Kontrollgrößen sind Mechanismus, Regio‑ und Stereoselektivität sowie die Einflüsse von Substituenten, Lösungsmittel und Katalysatoren.