Beispiele für Nukleophile sind Anionen wie Cl-, oder eine Verbindung mit einem einzelnen Elektronenpaar wie NH3 (Ammoniak).
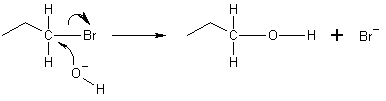
Im Beispiel unten gibt der Sauerstoff des Hydroxidions ein Elektronenpaar ab, das sich mit dem Kohlenstoff am Ende des Brompropanmoleküls verbindet. Die Bindung zwischen dem Kohlenstoff und dem Brom wird dann einer heterolytischen Spaltung unterzogen, wobei das Bromatom das gespendete Elektron aufnimmt und zum Bromidion (Br-) wird. Dies ist eine SN2-Reaktion, die durch Rückseitenangriff erfolgt. Dies bedeutet, dass das Hydroxid-Ion das Kohlenstoffatom von der anderen Seite angreift, genau gegenüber dem Brom-Ion. Aufgrund dieses Rückseitenangriffs führen SN2-Reaktionen zu einer Umkehrung der Konfiguration des Elektrophils. Wenn das Elektrophil chiral ist, behält es typischerweise seine Chiralität, obwohl die Konfiguration des SN2-Produkts im Vergleich zu der des ursprünglichen Elektrophils umgekehrt wird (Walden-Inversion).
Ein ambidentes Nukleophil ist ein Nukleophil, das von zwei oder mehr Orten aus angreifen kann, was zu zwei oder mehr Produkten führt. Zum Beispiel kann das Thiocyanation (SCN-) entweder vom S oder vom N aus angreifen. Aus diesem Grund führt die SN2-Reaktion eines Alkylhalogenids mit SCN- oft zu einer Mischung aus RSCN (einem Alkylthiocyanat) und RNCS (einem Alkylisothiocyanat). Ähnliche Mischungen werden bei der Kolbe-Nitrilsynthese auftreten.
Kohlenstoff-Nukleophile
Alkylmetallhalogenide sind Kohlenstoff-Nukleophile, die in der Grignard-Reaktion, Blaise-Reaktion, Reformatsky-Reaktion und Barbier-Reaktion, Organolithium-Reagenzien und Anionen eines terminalen Alkins vorkommen.
Auch Enole sind Kohlenstoff-Nukleophile. Die Bildung eines Enols wird durch Säure oder Base katalysiert. Enole sind ambidente Nukleophile, aber im Allgemeinen am Kohlenstoffatom neben den Kohlenstoffatomen mit Doppelbindung (Alphakohlenstoffatom) nukleophil. Enole werden häufig in Kondensationsreaktionen verwendet, einschließlich der Claisen-Kondensation und der Aldol-Kondensationsreaktionen.
Sauerstoff-Nukleophile
Beispiele für Sauerstoff-Nukleophile sind Wasser (H2O), Hydroxid-Anion, Alkohole, Alkoxid-Anionen, Wasserstoffperoxid und Carboxylat-Anionen.
Schwefel-Nukleophile
Von den Schwefelnukleophilen werden Schwefelwasserstoff und seine Salze, Thiole (RSH), Thiolat-Anionen (RS-), Anionen von Thiolcarbonsäuren (RC(O)-S-) und Anionen von Dithiocarbonaten (RO-C(S)-S-) und Dithiocarbamaten (R2N-C(S)-S-) am häufigsten verwendet.
Im Allgemeinen ist Schwefel aufgrund seiner großen Größe sehr nukleophil, was ihn leicht polarisierbar macht, und seine einzelnen Elektronenpaare sind leicht zugänglich.
Stickstoff-Nukleophile
Zu den Stickstoff-Nukleophilen gehören Ammoniak, Azid, Amine und Nitrite.
