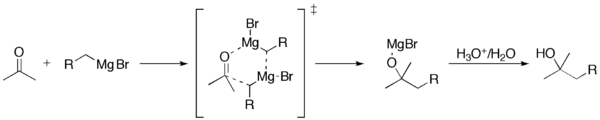
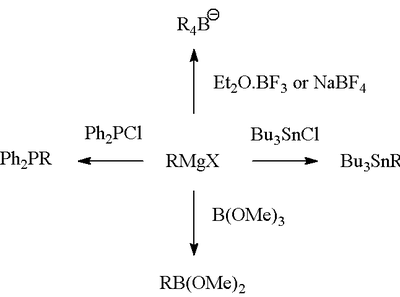
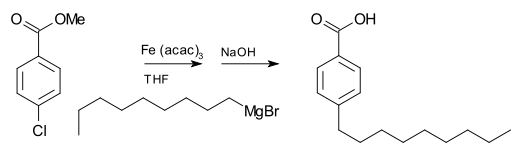
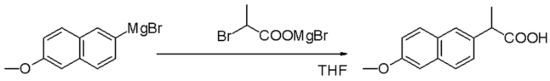
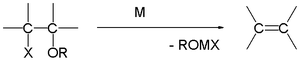
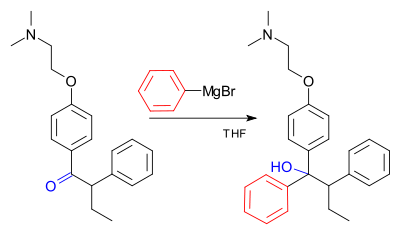
Die Grignard-Reaktion (ausgesprochen /ɡriɲar/) ist eine organometallische chemische Reaktion, bei der Alkyl- oder Aryl-Magnesiumhalogenide (Grignard-Reagenzien) elektrophile Kohlenstoffatome angreifen, die in polaren Bindungen vorhanden sind (z.B. in einer Carbonylgruppe wie im unten gezeigten Beispiel). Grignard-Reagenzien wirken als Nukleophile. Die Grignard-Reaktion erzeugt eine Kohlenstoff-Kohlenstoff-Bindung. Sie verändert die Hybridisierung um das Reaktionszentrum. Die Grignard-Reaktion ist ein wichtiges Werkzeug bei der Bildung von Kohlenstoff-Kohlenstoff-Bindungen. Sie kann auch Kohlenstoff-Phosphor-, Kohlenstoff-Zinn-, Kohlenstoff-Silizium-, Kohlenstoff-Bor- und andere Kohlenstoff-Heteroatom-Bindungen bilden.
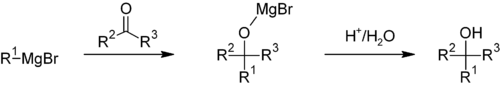
Es handelt sich um eine nukleophile organometallische Additionsreaktion. Der hohe pKa-Wert der Alkylkomponente (pKa = ~45) macht die Reaktion irreversibel. Grignard-Reaktionen sind nicht ionisch. Das Grignard-Reagenz liegt als organometallischer Cluster (in Ether) vor.
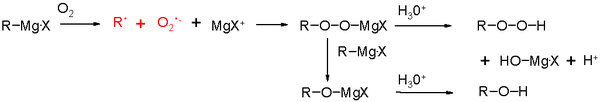
Der Nachteil von Grignard-Reagenzien ist, dass sie leicht mit protischen Lösungsmitteln (wie Wasser) oder mit funktionellen Gruppen mit sauren Protonen, wie Alkoholen und Aminen, reagieren. Atmosphärische Feuchtigkeit kann die Ausbeute bei der Herstellung eines Grignard-Reagenzes aus Magnesiumspänen und einem Alkylhalogenid verändern. Eine von vielen Methoden zum Ausschluss von Wasser aus der Reaktionsatmosphäre besteht darin, das Reaktionsgefäß flammtrocknen zu lassen, um die gesamte Feuchtigkeit zu verdampfen, die dann versiegelt wird, um eine Rückkehr der Feuchtigkeit zu verhindern. Die Chemiker verwenden dann Ultraschall, um die Oberfläche des Magnesiums zu aktivieren, so dass es eventuell vorhandenes Wasser verbraucht. Dadurch können sich Grignard-Reagenzien bilden, die weniger empfindlich auf vorhandenes Wasser reagieren.
Ein weiterer Nachteil der Grignard-Reagenzien ist, dass sie nicht ohne weiteres Kohlenstoff-Kohlenstoff-Bindungen bilden, indem sie mit Alkylhalogeniden über einen SN2-Mechanismus reagieren.
François Auguste Victor Grignard entdeckte Grignard-Reaktionen und -Reagenzien. Sie sind nach diesem französischen Chemiker (Universität Nancy, Frankreich) benannt, der für diese Arbeit 1912 den Nobelpreis für Chemie erhielt.