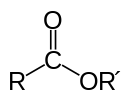
Ester sind organische Verbindungen mit der funktionellen Gruppe R–C(=O)–O–R′; man schreibt diese Gruppe oft als COOR. Ein Ester kann als ein Carbonyl mit einer Ether‑ähnlichen Bindung am Kohlenstoffatom beschrieben werden. Typischerweise werden Ester durch die saure Reaktion einer Carbonsäure mit einem Alkohol (Fischer‑Veresterung) und einem katalytischen Anteil an Säure hergestellt, wobei Wasser abgeht.
Allgemeine Eigenschaften
- Struktur: Allgemeine Summenformel R–C(=O)–O–R′ (COOR).
- Polarität und Siedepunkt: Ester sind polarer als entsprechende Ether, aber weniger polar als Alkohole; ihre Siedepunkte liegen häufig zwischen denen von Alkanen und Alkoholen vergleichbarer Molmasse.
- Geruch: Viele niedermolekulare Ester haben angenehme, oft fruchtige Gerüche (z. B. Ethylacetat, Methylbutyrat) und werden deshalb in Aromen und Parfüms eingesetzt.
- Reaktivität: Ester sind Carbonylverbindungen und reagieren vor allem über nukleophile Acylsubstitution (Hydrolyse, Transesterifizierung). Sie sind normalerweise weniger reaktiv als Säurechloride oder Anhydride, aber reaktiver als Amide.
Herstellung und wichtige Reaktionen
Die klassische Herstellung ist die Fischer‑Veresterung (säurekatalysierte Kondensation von Carbonsäure und Alkohol). Weitere gebräuchliche Methoden sind die Umsetzung von Carbonsäurechloriden oder Carbonsäureanhydriden mit Alkoholen, die Mitsunobu‑Reaktion, enzymatische Veresterungen und Kopplungen mit Aktivatoren (z. B. DCC bei Peptid‑/Ester‑Synthesen).
Ester können vielfältig reagieren:
- Hydrolyse: Saure Hydrolyse ist reversibel und liefert wieder Carbonsäure und Alkohol; basische Hydrolyse (Verseifung, Saponifikation) führt irreversibel zu Carboxylat‑Salzen und Alkoholen.
- Transesterifizierung: Austausch des Alkoxy‑Teils (–OR′) durch einen anderen Alkohol, katalysiert durch Säuren, Basen oder Enzyme (wichtig z. B. bei Biodiesel‑Herstellung).
- Reduktion: Ester lassen sich zu Ketonen oder zu Alkoholen reduzieren (z. B. LiAlH4 reduziert Ester zu zwei Alkoholen; DIBAL‑H kann selektiv zu Aldehyden reagieren; mit Organometallika kann nach Addition und Abspaltung ein Keton entstehen).
- Nukleophile Addition/Acylsubstitution: Ester können nukleophil angegriffen werden; die Additions‑Eliminations‑Mechanik ist ähnlich wie bei anderen Carbonsäurederivaten, jedoch oft etwas weniger leicht durchführbar als bei Ketonen.
- Claisen‑Kondensation: Enolate von Estern können zur Bildung von β‑Ketoestern kondensieren (wichtige Methode zur C–C‑Kettenverlängerung).
Nomenklatur
Nach IUPAC heißt ein Ester „Alkylalkanoat“ (z. B. Ethylacetat = Ethyl ethanoat). In der gebräuchlichen (trivialen) Nomenklatur wird oft der Alkyl‑Teil zuerst genannt (z. B. Methylbenzoat, Ethylacetat).
Vorkommen und Anwendungen
Ester sind eine sehr wichtige Funktionsgruppe und kommen in vielen Substanzen natürlichen und technischen Ursprungs vor. Sie sind sehr häufig in Fetten und Ölen enthalten: Triglyceride sind Triester aus Glycerin und Fettsäuren. Viele natürliche Duft‑ und Aromastoffe sind Ester (z. B. Methylbutyrat, Isoamylacetat).
- Lebensmittel und Parfüm: Ester werden als Aromen und Duftstoffe eingesetzt; sie liefern fruchtige Noten und finden Verwendung von Parfüms bis zu Aromen in Lebensmitteln.
- Kunststoffe: Polyester (z. B. PET) entstehen durch Veresterung/Polyesterbildung von Dicarbonsäuren mit Diolen; Polyester kommen deshalb in zahlreichen Kunststoffen vor.
- Industrielle Lösungsmittel: Ethylacetat, Butylacetat u. a. dienen als Lösungsmittel in Lacken, Klebstoffen und Extraktionen.
- Pharma und Agrochemie: Ester fungieren als Wirkstoff‑Gruppen oder Prodrugs (Veränderung von Lipophilie und Resorptionsverhalten).
- Biodiesel: Durch Transesterifizierung von Pflanzenölen mit Methanol/EtOH entstehen Methyl‑ bzw. Ethylester (= Biodiesel).
Nachweis und Spektroskopie
Es gibt viele Möglichkeiten, herauszufinden, ob ein Molekül eine Estergruppe hat. Die Infrarotspektroskopie liefert sehr scharfe Signale: typische C=O‑Dehnungsbanden bei einfachen Estern liegen um 1735–1750 cm−1 (verschiebbar bei Konjugation, Ringspannung oder H‑Brücken). Zusätzlich zeigen Ester starke C–O‑Streckungen im Bereich 1050–1300 cm−1.
Die Kohlenstoff‑NMR‑Spektroskopie (13C‑NMR) zeigt das Carbonyl‑C meist im Bereich ~160–185 ppm; im 1H‑NMR erscheinen Alkoxy‑gebundene Protonen (z. B. –OCH2–) typischerweise bei 3,5–4,5 ppm. In der Massenspektrometrie sind typische Fragmentierungen und McLafferty‑Umlagerungen beobachtbar.
Sicherheits‑ und Umweltaspekte
- Niedermolekulare Ester sind oft flüchtig und brennbar; gute Belüftung und Abstand von Zündquellen sind wichtig.
- Einige Ester können Hautreizungen oder Allergien auslösen; Sicherheitsdatenblätter beachten.
- Viele Ester sind biologisch abbaubar (insbesondere Fettsäureester), dennoch können Lösungsmittelester Umweltbelastungen verursachen, wenn sie großflächig freigesetzt werden.
Zusammenfassend sind Ester vielseitige und wichtige Verbindungen in Natur und Technik: Sie verbinden charakteristische physiko‑chemische Eigenschaften (Polarität, Geruch) mit einem breiten Reaktionsspektrum (Hydrolyse, Transesterifizierung, Reduktion, Kondensationen), was ihre Bedeutung in Chemie, Industrie, Pharmazie und Alltagsprodukten erklärt.