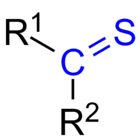
Definition und Struktur
Ein Thioketon (oder Thion) ist ein beliebiges Molekül mit der R2C=S-Gruppe. Es entspricht formal einem Keton, bei dem das Sauerstoffatom durch ein Schwefelatom ersetzt ist. Zwischen dem Kohlenstoffatom und dem Schwefel besteht eine Doppelbindung, das Schwefelatom trägt zusätzlich zwei einsame Paare. Durch die größere Atomgröße und die höhere Polarisierbarkeit des Schwefels unterscheidet sich die Bindungslänge und -stärke der C=S-Bindung deutlich von einer C=O-Bindung.
Warum sind Thioketone reaktiv?
Thioketone sind in vielen Fällen sehr reaktiv und oft weniger stabil als entsprechende Ketone. Dafür gibt es mehrere Gründe:
- Die p-p-Überlappung zwischen Kohlenstoff und Schwefel ist schlechter als zwischen Kohlenstoff und Sauerstoff, daher ist die π-Bindung des C=S energetisch schwächer.
- Schwefel ist stärker polarisierbar als Sauerstoff, was Thioketone zu weichen, leicht polarisierbaren Elektrophilen macht. Dadurch reagieren sie besonders gut mit geeigneten Nukleophilen und in perizyklischen Reaktionen.
- Viele Thioketone neigen zur Polymerisation oder zu Addition/Rekombination, wenn sie nicht durch sterische Hinderung oder Konjugation stabilisiert sind.
Typische Reaktionen
Wegen ihrer besonderen elektronischen Eigenschaften zeigen Thioketone eine Reihe charakteristischer Reaktionen:
- Cycloadditionsreaktionen: Thioketone dienen häufig als Dienophile in Diels-Alder-ähnlichen Reaktionen und bilden bevorzugt neue Ringe. Solche Cycloadditionen laufen oft schneller ab als bei entsprechenden Carbonylverbindungen.
- Nukleophile Addition: An der carbonylähnlichen C=S-Stelle können Nukleophile addieren und so z. B. Thioketale oder andere Additionsprodukte bilden.
- Weitere Umwandlungen: Thioketone lassen sich zu anderen Schwefelderivaten umsetzen (z. B. durch Oxidation oder Umsetzung mit Schwefeltransferreagenzien).
Thiale (Schwefel-Analoga der Aldehyde)
Wenn eine der R-Gruppen ein Wasserstoff ist, spricht man von der Schwefelvariante eines Aldehyds, einem Thial. Thiale sind in der Regel noch reaktiver als Thioketone: sie sind besonders anfällig für Additionsreaktionen und Polymerisation und weisen oft ausgeprägten Geruch.
Herstellung und Beispiele
Thioketone lassen sich in der Praxis häufig durch Thionierung von Ketonen gewinnen, also durch Austausch des Sauerstoffs gegen Schwefel. Übliche Reagenzien für solche Umsetzungen sind z. B. Lawesson-Reagenz oder Phosphorpentasulfid (P4S10). Manche Thioketone sind nur kurzlebig, andere, wie z. B. sterisch geschützte oder konjugierte Verbindungen (z. B. Thiobenzophenon-Derivate), sind isolierbar und dienen in der organischen Synthese als reaktive Bausteine.
Vergleich zu Ketonen
Im Vergleich zu normalen Ketonen zeigen Thioketone:
- größere Polarisi ebar keit und damit andere Reaktivitätsmuster,
- häufig erhöhte Reaktionsgeschwindigkeiten in Cycloadditions- und Additionsreaktionen,
- andere spektroskopische Eigenschaften (z. B. verschobene IR- und NMR-Signale für die C=S-Einheit).
Stabilisierung, Anwendung und Sicherheit
Stabilität von Thioketonen lässt sich durch konjugierende Substituenten oder durch sterische Abschirmung erhöhen. In der Forschung werden stabilere Thioketone als reaktive Bausteine für Cycloadditionen und in der Materialchemie genutzt. Viele Thione und besonders Thiale haben einen starken, unangenehmen Geruch und können reizend oder toxisch sein; daher sind beim Umgang geeignete Schutzmaßnahmen (Abzug, Handschuhe) notwendig.
Zusammenfassend sind Thioketone interessante, elektronisch vom Keton verschiedene Verbindungen mit ausgeprägter Reaktivität, die sich besonders in Cycloadditions‑ und Additionsreaktionen zeigen. Ihre Chemie wird durch die Eigenschaften des Schwefels – größere Größe, hohe Polarisierbarkeit und schwächere π‑Überlappung – bestimmt.