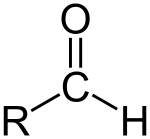
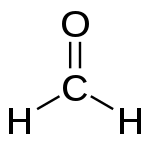
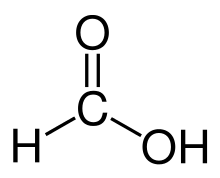
Ein Aldehyd (/ˈældɪhaɪd/) ist eine organische Verbindung. Es enthält eine Formylgruppe. Eine Formylgruppe ist ein Teil eines Moleküls mit der Struktur R-CHO. Sie besteht aus einem Kohlenstoff, der doppelt an Sauerstoff gebunden ist. Der Sauerstoff ist auch an Wasserstoff und eine R-Gruppe gebunden. Eine Seitenkette ist der Rest des Moleküls. Die Gruppe ohne die Seitenkette wird als Aldehydgruppe oder Formylgruppe bezeichnet. Aldehyde unterscheiden sich von Ketonen, da sich die Formylgruppe am Ende des Moleküls in einem Aldehyd befindet. Bei Ketonen befindet sich die Formylgruppe in der Mitte des Moleküls. Aldehyde sind in der organischen Chemie weit verbreitet. Viele Duftstoffe (geruchsbildende Verbindungen) sind Aldehyde.
Aldehyde
Struktur und Bindung
Aldehyde haben einen Kohlenstoff, der doppelt an einen Sauerstoff gebunden ist. Dadurch sind sie leicht polar. Dadurch haben Aldehyde eine Reihe von Eigenschaften. Eine der wichtigsten davon ist die Löslichkeit in Wasser.
Nomenklatur
IUPAC-Namen für Aldehyde
Die gebräuchlichen Namen für Aldehyde sind nicht immer die offiziellen Namen. Die IUPAC-Namen sind jedoch nützlich. Die IUPAC empfiehlt die folgende Nomenklatur für Aldehyde:
- Aldehyde ohne Kohlenstoffringe werden auf der Grundlage der längsten Kohlenstoffkette, die den Aldehyd enthält, benannt. So wird HCHO auf der Basis von Methan und CH3CH2CH2CH2CHO auf der Basis von Butan benannt. Der Name wird durch Änderung der Endung -e des Stammalkans in -al gebildet. HCHO wird auf der Basis von Methanal benannt. CH3CH2CH2CH2CHO wird als Butanal bezeichnet.
- Wenn eine -CHO-Gruppe an einen Ring gebunden ist, dann wird -Carbaldehyd an das Ende des Namens angefügt. Aus diesem Grund ist C6H11CHO als Cyclohexancarbaldehyd bekannt. Wenn es andere Namen gibt, die an das Wortende angefügt werden müssen, weil andere funktionelle Gruppen vorhanden sind, wird Formyl- an den Wortanfang angefügt. Methanoyl- wird manchmal stattdessen hinzugefügt, aber Formyl- ist besser.
Etymologie
Das Wort Aldehyd kommt aus dem Lateinischen. Es wurde von alcohol dehydrogenatus (dehydrierter Alkohol) abgekürzt. Das Wort Aldehyd wurde von Justus von Liebig geschaffen. In der Vergangenheit wurden Aldehyde manchmal nach den entsprechenden Alkoholen benannt, z.B. Weinaldehyd für Acetaldehyd. (Vinous stammt vom lateinischen Wort für Wein, der traditionellen Quelle für Ethanol).
Der Begriff Formylgruppe stammt vom lateinischen oder italienischen Wort formica, was Ameise bedeutet.
Physikalische Eigenschaften und Charakterisierung
Aldehyde haben viele verschiedene Eigenschaften. Diese Eigenschaften ändern sich sehr stark, wenn sich der Rest des Moleküls ändert. Kleinere Aldehyde sind in Wasser besser löslich. Formaldehyd und Acetaldehyd sind in Wasser vollständig löslich. Viele Aldehyde haben starke Gerüche. Aldehyde werden an der Luft abgebaut.
Zwei der wichtigsten Aldehyde, Formaldehyd und Acetaldehyd, neigen dazu, lange Ketten zu bilden. Dies nennt man Polymerisation.
Natürlich vorkommende Aldehyde
Viele Aldehyde kommen in ätherischen Ölen vor und sind der Grund für ihre Gerüche. Zimtaldehyd, Koriander und Vanillin riechen alle nach Aldehyden.
Häufige Reaktionen
Aldehyde sind hoch reaktiv und an vielen Reaktionen beteiligt". In der Industrie werden Aldehyde zur Herstellung von Weichmachern, Polyolen und Alkoholen verwendet. In der Biologie werden Aldehyde verwendet, um Amingruppen zu ersetzen und Zucker zu bilden.
Dialdehyde
Ein Dialdehyd ist ein Molekül mit zwei Aldehyden. Die Namen von Dialdehyden haben die Endung -dial oder -dialdehyd. Einige Dialdehyde sind nach der Säure benannt, der sie ähnlich sind. Ein Beispiel ist Butanedial, das auch als Succinaldehyd (von Bernsteinsäure) bezeichnet wird.
Beispiele für Aldehyde
- Methanal (Formaldehyd)
- Ethanal (Acetaldehyd)
- Propanal (Propionaldehyd)
- Butanal (Butyraldehyd)
- Benzaldehyd
- Zimtaldehyd
- Tolualdehyd
- Furfural
- Retinaldehyd
Dialdehyde
- Glyoxal
- Malondialdehyd
- Succindialdehyd
- Glutaraldehyd
- Phthalaldehyd
Verwendet
Von allen Aldehyden wird Formaldehyd am meisten produziert. Es werden etwa 6 Millionen Tonnen pro Jahr hergestellt. Es wird hauptsächlich zur Herstellung von Harzen verwendet, wenn es mit Harnstoff, Melamin und Phenol gemischt wird. Bakelit wird auf diese Weise hergestellt. Ein weiteres häufig hergestelltes Aldehyd ist Butyraldehyd. Es werden 2,5 Millionen Tonnen pro Jahr hergestellt. Einst wurde viel Acetaldehyd hergestellt, aber heute wird viel weniger hergestellt. Das liegt daran, dass Chemikalien, die früher aus Acetaldehyd hergestellt wurden, heute auf andere Weise hergestellt werden.
Verwandte Seiten
Fragen und Antworten
F: Was ist ein Aldehyd?
A: Ein Aldehyd ist eine organische Verbindung, die eine Formylgruppe enthält.
F: Was ist eine Formylgruppe?
A: Eine Formylgruppe ist ein Teil eines Moleküls mit der Struktur R-CHO, das aus einem Kohlenstoff besteht, der doppelt an Sauerstoff gebunden ist und auch an Wasserstoff und eine R-Gruppe gebunden ist.
F: Was ist eine Seitenkette in einem Molekül?
A: Eine Seitenkette ist der Rest des Moleküls mit Ausnahme der funktionellen Gruppe.
F: Was ist die funktionelle Gruppe in einem Aldehyd?
A: Die funktionelle Gruppe in einem Aldehyd ist die Aldehydgruppe oder Formylgruppe.
F: Wie unterscheiden sich Aldehyde von Ketonen?
A: Die Formylgruppe in Aldehyden befindet sich am Ende des Moleküls, während sie sich in Ketonen in der Mitte befindet.
F: Welche Bedeutung haben Aldehyde in der organischen Chemie?
A: Aldehyde sind in der organischen Chemie weit verbreitet und werden in vielen Reaktionen als Reaktanten oder Zwischenprodukte verwendet.
F: Wie werden Aldehyde häufig verwendet?
A: Viele Parfüms, wie Chanel No. 5, bestehen aus Aldehyden. Sie können als Konservierungsmittel in Lebensmitteln verwendet werden. Sie werden als Zwischenprodukte bei der Herstellung von Arzneimitteln, Farbstoffen und anderen Chemikalien verwendet.