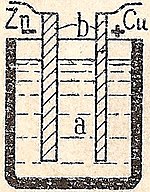
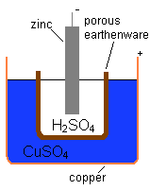
Eine elektrochemische Zelle, die einen externen elektrischen Stromfluss verursacht, kann mit zwei verschiedenen Metallen hergestellt werden, da Metalle sich in ihrer Neigung, Elektronen zu verlieren, unterscheiden. Zink verliert leichter Elektronen als Kupfer, so dass das Einbringen von Zink und Kupfermetall in Lösungen ihrer Salze dazu führen kann, dass Elektronen durch einen externen Draht fließen, der vom Zink zum Kupfer führt. Wenn ein Zinkatom die Elektronen liefert, wird es zu einem positiven Ion und geht in wässrige Lösung, wodurch die Masse der Zinkelektrode verringert wird. Auf der Kupferseite ermöglichen es die beiden erhaltenen Elektronen, ein Kupferion aus der Lösung in ein ungeladenes Kupferatom umzuwandeln, das sich auf der Kupferelektrode niederschlägt, wodurch die Masse der Kupferelektrode erhöht wird. Die beiden Reaktionen werden typischerweise geschrieben
Zn(s) --> Zn2+(aq) + 2e-
Cu2+(aq) + 2e- --> Cu(s)
Die Buchstaben in Klammern erinnern nur daran, dass das Zink von einem Festkörper (s) in eine wässrige Lösung (aq) übergeht und umgekehrt für das Kupfer. Es ist typisch in der Sprache der Elektrochemie, diese beiden Prozesse als "Halbreaktionen" zu bezeichnen, die an den beiden Elektroden ablaufen.
| Zn(s) -> Zn2+(aq) + 2e- | | Die "Halbreaktion" von Zink wird als Oxidation klassifiziert, da sie Elektronen verliert. Der Endpunkt, an dem die Oxidation stattfindet, wird als "Anode" bezeichnet. Bei einer Batterie ist dies der Minuspol. | |
| Die Kupfer-"Halbreaktion" wird als Reduktion klassifiziert, da sie Elektronen gewinnt. Die Klemme, an der die Reduktion stattfindet, wird als "Kathode" bezeichnet. Bei einer Batterie ist dies der positive Pol. | | Cu2+(aq) + 2e- -> Cu(s) |
Damit die Voltaik-Zelle weiterhin einen externen elektrischen Strom erzeugen kann, muss eine Bewegung der in Lösung befindlichen Sulfationen von rechts nach links erfolgen, um den Elektronenfluss im externen Stromkreis auszugleichen. Die Metallionen selbst müssen daran gehindert werden, sich zwischen den Elektroden zu bewegen, daher muss eine Art poröse Membran oder ein anderer Mechanismus für die selektive Bewegung der negativen Ionen im Elektrolyten von rechts nach links sorgen.
Energie wird benötigt, um die Elektronen zu zwingen, sich von der Zink- zur Kupferelektrode zu bewegen, und die Menge an Energie pro Ladungseinheit, die von der voltaischen Zelle zur Verfügung steht, wird als elektromotorische Kraft (EMK) der Zelle bezeichnet. Die Energie pro Ladungseinheit wird in Volt ausgedrückt (1 Volt = 1 Joule/Coulomb).
Es liegt auf der Hand, dass man, um Energie aus der Zelle zu gewinnen, mehr Energie aus der Oxidation des Zinks freisetzen muss, als zur Reduktion des Kupfers nötig ist. Die Zelle kann aus diesem Prozess eine endliche Menge an Energie gewinnen, wobei der Prozess durch die Menge des entweder im Elektrolyten oder in den Metallelektroden verfügbaren Materials begrenzt ist. Befindet sich beispielsweise ein Mol der Sulfationen SO42- auf der Kupferseite, dann beschränkt sich der Prozess auf die Übertragung von zwei Mol Elektronen durch den externen Stromkreis. Die Menge der elektrischen Ladung, die in einem Mol Elektronen enthalten ist, wird als Faraday-Konstante bezeichnet und ist gleich der Avogadro-Zahl mal der Elektronenladung:
Faraday-Konstante = F = NAe = 6,022 x 1023 x 1,602 x 10-19 = 96.485 Coulombs/Mol
Die Energieausbeute einer voltaischen Zelle ergibt sich aus der Zellspannung mal der Anzahl der übertragenen Elektronenmol mal der Faraday-Konstante.
Elektrische Energieleistung = nFE-Zelle
Die Zell-EMK-Zelle kann aus den Standardelektrodenpotentialen für die beiden Metalle vorhergesagt werden. Für die Zink/Kupfer-Zelle beträgt das berechnete Zellpotential unter den Standardbedingungen 1,1 Volt.