Eine Cycloaddition ist eine chemische Reaktion zwischen Reaktanten mit Doppelbindungen, die durch eine Ringstruktur ersetzt werden. Es handelt sich um eine pericyclische chemische Reaktion, bei der sich "zwei oder mehr ungesättigte Moleküle (oder Teile desselben Moleküls) mit der Bildung eines cyclischen Addukts verbinden, in dem es zu einer Nettoreduktion der Bindungsvielfalt kommt". Es handelt sich um eine zyklische Reaktion: Es entsteht ein neuer Ring aus Atomen. Pericyclische Reaktionen laufen in der Regel konzertiert ab, das heißt, Bindungen werden in einem einzigen, zusammenhängenden Schritt umorganisiert; dies führt oft zu hoher Stereospezifität der Produkte. Die Betrachtung der beteiligten π-Orbitale und ihrer Symmetrien (Woodward–Hoffmann-Regeln) erklärt, welche Cycloadditionen thermisch oder photochemisch erlaubt sind.
Cycloadditionen werden nach der Grundgröße der Moleküle benannt, die zusammengebracht werden. Damit wäre die Diels-Alder-Reaktion eine [4 + 2]-Cycloaddition und die 1,3-dipolare Cycloaddition eine [3 + 2]-Cycloaddition. Diese Art von Reaktion ist eine unpolare Additionsreaktion.
Grundprinzipien und Mechanismus
Bei pericyclischen Cycloadditionen erfolgt der Elektronentransfer in einem zyklischen Übergangszustand. Wichtige Konzepte sind:
- Frontier-MO-Theorie (FMO): Die Wechselwirkung zwischen dem HOMO eines Reaktanten und dem LUMO des anderen kontrolliert Reaktivität, Regio- und Stereoselektivität. Ein elektronreiches Diene und ein elektronarmes Dienophil beschleunigen beispielsweise die Diels-Alder-Reaktion.
- Woodward–Hoffmann-Regeln: Bestimmen, welche Kombinationen von suprafazialen/antarafazialen Verschiebungen thermisch bzw. photochemisch erlaubt sind. Klassische [4+2]-Diels–Alder-Reaktionen sind thermisch allowed (suprafazial an beiden Komponenten).
- Konzertiert vs. schrittweise: Viele Cycloadditionen sind konzertiert; unter bestimmten Bedingungen (z. B. bei stark substituierten Systemen oder besonderen Substituenten) können zwischengeschaltete Radikal- oder Ionenzustände auftreten.
Stereochemie und Regioselektivität
Cycloadditionen sind häufig stereospezifisch: stereochemische Informationen in den Edukten werden in das Produkt überführt. Wichtige Aspekte sind:
- Endo-/Exo-Regel (bei Diels–Alder): Bei vielen dienophile Substituenten wird das endo-Produkt bevorzugt, weil sekundäre Wechselwirkungen im Übergangszustand stabilisierend wirken (klassisch: Cyclopentadien + Maleinsäureanhydrid → überwiegend endo-Produkt).
- Regioselektivität: Elektronenziehende bzw. -schiebende Substituenten führen zu bevorzugter Orientierung, die sich mit Hilfe der FMO-Analyse vorhersagen lässt.
- Stereospezifität: Trans- bzw. cis-Anordnungen in den Ausgangsmaterialien führen meist zu entsprechend trans-/cis-substituierten Produkten.
Typen von Cycloadditionen — Beispiele
- Diels–Alder (4+2): Diene + Dienophil → cyclohexenartige Produkte. Häufig eingesetzt in der Synthese komplexer Naturstoffe. Typisches Beispiel: Cyclopentadien + Maleinsäureanhydrid.
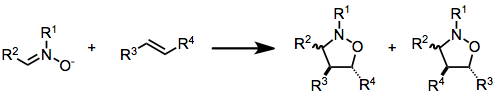
- 1,3-Dipolare Cycloaddition (3+2): Ein 1,3-Dipol (z. B. Nitrilon, Nitriloxid, Azomethinylid) reagiert mit einem Dipolarophil (Alken/Alkin) zu fünfgliedrigen Heterocyclen. Beispiele: Bildung von Isoxazolen, Isoxazolidinen oder 1,2,3-Triazolen.
- Cheletrope Reaktionen: Sonderfall, bei dem beide neuen Bindungen zu demselben Atom gebildet werden (z. B. SO2-Addition an ein Cyclopentadienylid).
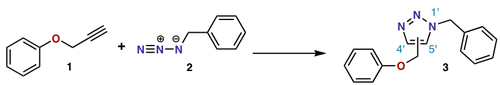
- Azid-Alkin-Cycloaddition (Huisgen, „Click“): Die thermische 1,3-dipolare Cycloaddition von Aziden und Alkinen liefert 1,2,3-Triazole; die kupferkatalysierte Variante (CuAAC) ist eine extrem nützliche, schnelle und regioselektive Methode in der „Click“-Chemie (führt bevorzugt zu 1,4-substituierten Triazolen).
Katalyse, Bedingungen und praktische Hinweise
- Lewis-Säuren (z. B. AlCl3, BF3·OEt2) aktivieren Dienophile, indem sie deren LUMO absenken und so Reaktionsgeschwindigkeit und Selektivität erhöhen.
- Temperatur und Lösungsmittel: Höhere Temperaturen beschleunigen oft die Reaktion, können aber Selektivität verringern; polare Lösungsmittel können polare Charaktere verstärken und so Reaktionsraten beeinflussen.
- Photochemische Aktivierung: Unter Bestrahlung können sonst thermisch verbotene Pfade zugänglich werden oder umgekehrt die Reaktivität verändern (andere Orbital-Symmetriebedingungen gelten).
- Katalysierte Varianten: Neben Lewis-Säuren gibt es Metallkatalysen und organokatalytische Konzepte, die z. B. regio- und enantioselektive Cycloadditionen ermöglichen.
Anwendungen
Cycloadditionen sind in der organischen Synthese außerordentlich wichtig:
- Synthese komplexer Naturstoffe und Pharmaka durch Aufbau ringförmiger Gerüste in wenigen Schritten.
- Materialwissenschaften: Herstellung von funktionellen Polymeren und Vernetzungen (z. B. durch Diels–Alder-Click-Verknüpfungen).
- Biokonjugation: CuAAC als robustes Werkzeug zum Kopplen von Biomolekülen.
Kurze Zusammenfassung
- Cycloadditionen bauen Ringe auf und laufen oft konzertiert (pericyclisch) ab.
- Die Bezeichnung [m+n] gibt die Anzahl der π-Elektronen bzw. Atome der addierenden Fragmente an (z. B. [4+2], [3+2]).
- FMO-Theorie und Woodward–Hoffmann-Regeln erklären Reaktivität, Selektivität und erlaubte Reaktionspfade.
- Praktisch wichtig sind Diels–Alder, 1,3-dipolare Cycloaddition und die kupferkatalysierte Azid‑Alkin‑Cycloaddition („Click“).
Bei speziellen Fragestellungen (z. B. detaillierte FMO-Analysen, stereochemische Vorhersagen für konkrete Substrate oder experimentelle Bedingungen) kann ich gern konkrete Beispiele und Mechanismusdiagramme erläutern.
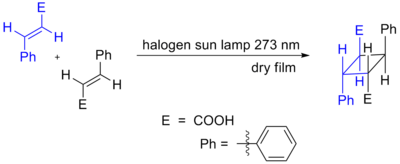
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)