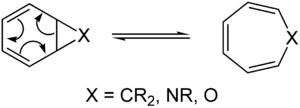
In der organischen Chemie ist eine pericyclische Reaktion eine Art chemische Reaktion zwischen organischen Verbindungen. Im Falle von pericyclischen Reaktionen ist der Übergangszustand des Moleküls ein Ring (hat eine zyklische Geometrie), und die Reaktion verläuft konzertiert. Pericyclische Reaktionen sind in der Regel Umlagerungsreaktionen. Die wichtigsten Gruppen von pericyclischen Reaktionen sind:
- Elektrozyklische Reaktionen
- Cycload-Ausgaben
- Sigmatropische Reaktionen
- Gruppentransfer-Reaktionen
- Cheletropische Reaktionen
- Dyotrope Reaktionen
Pericyclische Reaktionen sind im Allgemeinen Gleichgewichtsprozesse. Es ist jedoch möglich, die Reaktion in eine Richtung zu schieben, wenn sich das Produkt auf einem deutlich niedrigeren Energieniveau befindet. Damit wird das Prinzip von Le Chatelier auf eine Reaktion mit einem einzigen Molekül angewandt.
Mit vielen perizyklischen Reaktionen sind ähnlich schrittweise radikale Prozesse verbunden. Chemiker sind sich nicht einig, ob einige Reaktionen pericyclische Reaktionen sind. So ist z.B. nicht definitiv bekannt, ob der [2+2] Cycloaddition-Mechanismus konzertiert ist (oder vom reaktiven System abhängen kann). Viele pericyclische Reaktionen haben ähnliche Reaktionen, die durch Metalle katalysiert werden. Aber auch diese metallkatalysierten Reaktionen sind nicht wirklich pericyclisch. Die Metallkatalysatoren stabilisieren die Reaktionszwischenprodukte. Die Reaktion ist also nicht konzertiert, sondern eher metallstabilisiert.
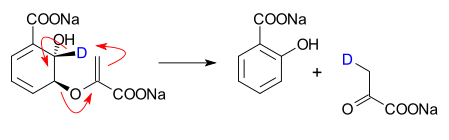
Eine große photoinduzierte Wasserstoff-Sigmatropieverschiebung wurde in einer von Albert Eschenmoser durchgeführten Corrinsynthese mit einem 16π System genutzt.
Aufgrund des Prinzips der mikroskopischen Reversibilität gibt es einen parallelen Satz von "retro" pericyclischen Reaktionen, die die umgekehrte Reaktion durchführen.