Eine sigmatrope Reaktion in der organischen Chemie ist eine pericyclische Reaktion. Bei einer sigmatropen Reaktion wird kein Katalysator verwendet und es handelt sich um ein einzelnes Molekül (ein unkatalysierter intramolekularer Prozess). Dabei wird eine σ-Bindung in eine andere σ-Bindung umgewandelt. Der Name sigmatropic ist das Ergebnis einer Verbindung aus dem seit langem etablierten Namen "sigma" für Kohlenstoff-Kohlenstoff-Einzelbindungen und dem griechischen Wort tropos, was Wende bedeutet. Dabei handelt es sich um eine Umlagerungsreaktion, was bedeutet, dass sich die Bindungen in einem Molekül zwischen den Atomen verschieben, ohne dass Atome das Molekül verlassen oder neue Atome hinzugefügt werden. In einer sigmatropen Reaktion bewegt sich ein Substituent in einer intramolekularen Reaktion von einem Teil eines π-gebundenen Systems zu einem anderen Teil bei gleichzeitiger Umordnung des π-Systems. Echte sigmatrope Reaktionen benötigen normalerweise keinen Katalysator. Einige sigmatrope Reaktionen werden durch eine Lewis-Säure katalysiert. Sigmatrope Reaktionen haben oft Übergangsmetallkatalysatoren, die in analogen Reaktionen Zwischenprodukte bilden. Die bekanntesten der sigmatropen Umlagerungen sind die [3,3] Cope-Umlagerung, Claisen-Umlagerung, Carroll-Umlagerung und die Fischer-Indolsynthese.
Sigmatrope Umlagerung
Überblick über Sigmatropische Verschiebungen
Woodward-Hoffman Nomenklatur der Sigmatropischen Verschiebung
Für die Beschreibung sigmatropischer Verschiebungen wird eine spezielle Notation verwendet. Jedem der Kohlenstoffatome auf dem Rückgrat des Moleküls ist eine Positionsnummer zugeordnet. Sigmatrope Rearrangements werden durch einen Ordnungsbegriff [i,j] beschrieben. Dies bedeutet die Wanderung einer σ-Bindung, die an ein oder mehrere π Systeme angrenzt, an eine neue Position (i-1) und (j-1) Atome, die von der ursprünglichen Position der σ-Bindung entfernt sind. Wenn die Summe von i und j eine gerade Zahl ist, ist dies ein Hinweis auf die Beteiligung einer neutralen, alle C-Atome umfassenden Kette. Eine ungerade Zahl deutet darauf hin, dass ein geladenes C-Atom oder ein einzelnes Heteroatompaar vorhanden ist, das eine Kohlenstoff-Kohlenstoff-Doppelbindung ersetzt. So werden [1,5]- und [3,3]-Verschiebungen zu [1,4]- und [2,3]-Verschiebungen mit Heteroatomen, wobei die Symmetrieerwägungen gewahrt bleiben. Im dritten Beispiel werden aus Gründen der Klarheit die Wasserstoffatome weggelassen.

Hier ist ein Weg, die Reihenfolge einer gegebenen sigmatropischen Neuanordnung zu finden. Der erste Schritt besteht darin, jedem Atom Zahlen zu geben, beginnend mit den Atomen der unterbrochenen Bindung als Atom 1. Chemiker zählen die Atome in jeder Richtung von der unterbrochenen Bindung bis zu den Atomen, die die neue σ-Bindung im Produkt bilden. Die Zahlen, die den Atomen entsprechen, die die neue Bindung bilden, werden dann durch ein Komma getrennt und in Klammern gesetzt. Dadurch entsteht der sigmatrope Deskriptor der Reaktionsordnung.
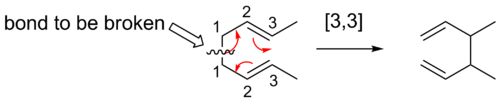
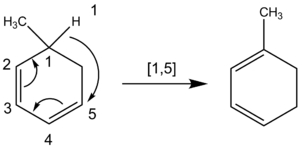
Chemiker zählen auch Atome, wenn sie eine sigmatropische Verschiebung benennen, bei der sich ein Wasserstoffatom bewegt. Die Kohlenstoffkette bricht nicht bei einer Wasserstoff-Atomwanderung. Chemiker zählen also über alle an der Reaktion beteiligten Atome und nicht nur über die nächstgelegenen Atome. Beispielsweise hat die folgende Wasserstoffatomwanderung die Ordnung [1,5], die durch Zählen gegen den Uhrzeigersinn durch das π System erreicht wird, und nicht die Ordnung [1,3] durch die CH2-Ringgruppe, die sich fälschlicherweise ergeben würde, wenn im Uhrzeigersinn gezählt würde.
Suprafaziale und antarafaziale Verschiebungen
Chemiker haben sigmatropische Reaktionen untersucht, bei denen die wandernde Gruppe ein Sterozentrum hat. Im Prinzip können alle sigmatropen Verschiebungen entweder mit der gleichen (Retention) oder der entgegengesetzten (Inversion) Geometrie der wandernden Gruppe auftreten. Dies hängt davon ab, ob der ursprüngliche Bindungslappen des migrierenden Atoms oder dessen anderer Lappen zur Bildung der neuen Bindung verwendet wird.
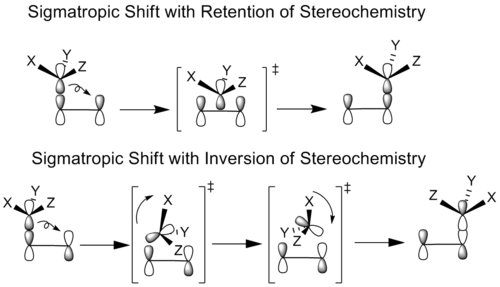
In Fällen von stereochemischer Retention übersetzt die wandernde Gruppe ohne Rotation in die Bindungsposition. Im Falle einer stereochemischen Inversion rotiert und translatiert die migrierende Gruppe sowohl, um ihre gebundene Konformation zu erreichen.
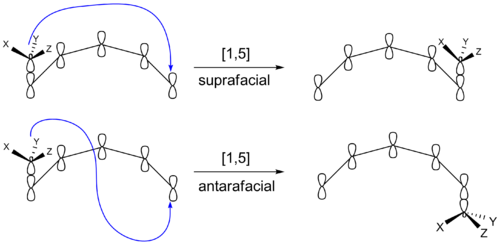
Es gibt eine weitere Möglichkeit, dass eine sigmatrope Reaktion Produkte mit unterschiedlicher Sterochemie erzeugen kann. Die migrierende Gruppe kann nach der Wiederzusammenführung auf dem ursprünglichen Gesicht des π Systems bleiben. Oder sie kann auf die gegenüberliegende Seite des π Systems gehen. Wenn die migrierende Gruppe auf der gleichen Seite des π Systems bleibt, wird die Verschiebung als suprafazial bezeichnet. Wenn die migrierende Gruppe auf das gegenüberliegende Gesicht wechselt, spricht man von einer antarafazialen Verschiebung. Transformationen, die innerhalb kleiner oder mittlerer Ringe stattfinden, können keine antarafazialen Verschiebungen vornehmen.
Klassen von sigmatropischen Umordnungen
[1,3] Schichten
Thermische Hydrid-Verschiebungen
Bei einer thermischen [1,3] Hydridverschiebung bewegt ein Hydrid drei Atome. Die Woodward-Hoffmann-Regeln schreiben vor, dass es in einer antarafazialen Verschiebung abläuft. Obwohl eine solche Verschiebung Symmetrie erlaubt ist, verbietet die im Übergangszustand erforderliche Mobius-Topologie eine solche Verschiebung. Sie ist geometrisch unmöglich. Aus diesem Grund isomerisieren Enole nicht ohne einen sauren oder basischen Katalysator.
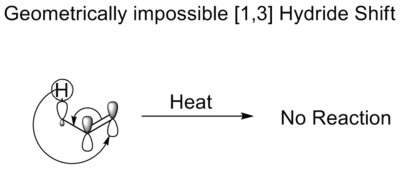
Thermische Alkyl-Verschiebungen
Thermische Alkyl [1,3]-Verschiebungen, ähnlich wie [1,3]-Hydridverschiebungen, müssen antarafazial verlaufen. Die Geometrie des Übergangszustands ist prohibitiv. Aber eine Alkylgruppe kann aufgrund der Beschaffenheit ihrer Orbitale ihre Geometrie umkehren und eine neue Bindung mit dem Rückenlappen ihres sp3-Orbitals bilden. Diese Reaktion führt zu einer suprafazialen Verschiebung. Diese Reaktionen sind in offenen Kettensystemen wegen der stark geordneten Natur des Übergangszustands immer noch nicht üblich. Daher funktionieren die Reaktionen in zyklischen Molekülen besser.
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
Fotochemische [1,3] Verschiebungen
Photochemische [1,3] Verschiebungen sollten suprafaziale Verschiebungen sein; die meisten sind jedoch nicht konzertiert, weil sie durch einen Triplett-Zustand verlaufen (d.h. sie haben einen diradikalen Mechanismus, auf den die Woodward-Hoffmann-Regeln nicht anwendbar sind).
[1,5] Schichten
Eine [1,5]-Verschiebung beinhaltet die Verschiebung von 1 Substituenten (-H, -R oder -Ar) um 5 Atome eines π Systems nach unten. Es hat sich gezeigt, dass sich Wasserstoff sowohl in zyklischen als auch in offenen Kettensystemen bei Temperaturen von 200 oder mehr verschiebt ˚C. Es wird vorhergesagt, dass diese Reaktionen suprafazial ablaufen, durch einen Übergangszustand nach der Huckel-Topologie.
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
Eine Photobestrahlung würde eine antarafaziale Verschiebung von Wasserstoff erfordern. Obwohl solche Reaktionen selten sind, gibt es Beispiele, bei denen antarafaziale Verschiebungen begünstigt werden:
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)
Im Gegensatz zu Wasserstoff [1,5]-Verschiebungen wurden in einem offenkettigen System noch nie [1,5]-Alky-Verschiebungen beobachtet. Chemiker haben Ratenpräferenzen für [1,5] Alkylverschiebungen in zyklischen Systemen ermittelt: Carbonyl und Carboxyl> Hydrid> Phenyl und Vinyl>> Alkyl.
Alkylgruppen durchlaufen [1,5] Verschiebungen sehr schlecht und benötigen in der Regel hohe Temperaturen. Für Cyclohexadiene ist die Temperatur für Alkylverschiebungen jedoch nicht viel höher als die für Carbonyle, die beste wandernde Gruppe. Eine Studie zeigte, dass dies darauf zurückzuführen ist, dass die Alkylverschiebungen an Cyclohexadienen durch einen anderen Mechanismus ablaufen. Zuerst öffnet sich der Ring, gefolgt von einer [1,7]-Verschiebung, und dann reformiert sich der Ring elektrozyklisch:
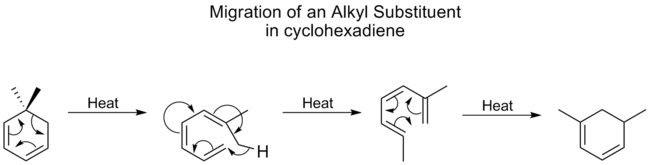
Derselbe mechanistische Prozess wird weiter unten, ohne die abschließende elektrozyklische Ringschlussreaktion, bei der Interkonversion von Lumisterol in Vitamin D2 gesehen.
[1,7] Schichten
[1,7] sigmatropische Verschiebungen werden durch die Woodward-Hoffmann-Regeln vorhergesagt, um antarafazial zu verlaufen, durch einen Mobius-Topologie-Übergangszustand. Eine antarafaziale [1,7] Verschiebung wird bei der Umwandlung von Lumisterol in Vitamin D2 beobachtet, wobei sich nach einer elektrozyklischen Ringöffnung zum Prävitamin D2 ein Methylwasserstoff verschiebt.
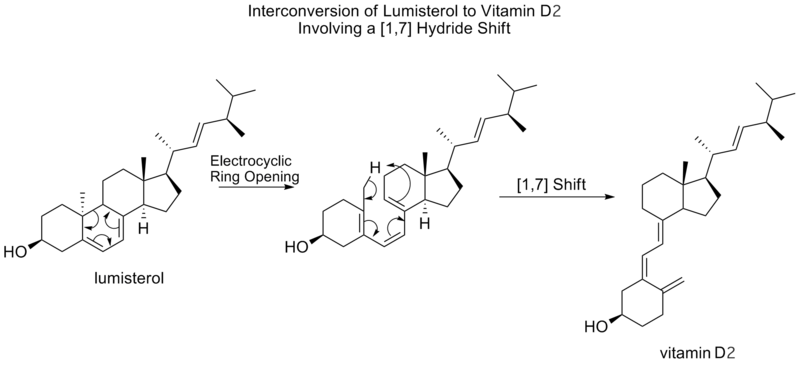
Bicyclische Nonatriene unterliegen ebenfalls [1,7] Verschiebungen in einer so genannten Walk-Rearrangement, d.h. der Verschiebung einer zweiwertigen Gruppe als Teil eines dreigliedrigen Rings in einem bicyclischen Molekül.
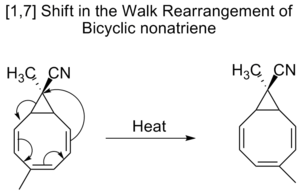
[3,3] Schichten
[3,3] Sigmatropische Verschiebungen sind gut untersuchte sigmatropische Rearrangements. Die Woodward-Hoffman-Regeln sagen voraus, dass diese sechs Elektronenreaktionen suprafazial verlaufen würden, wobei ein Huckel-Topologie-Übergangszustand verwendet wird.
Claisen-Umgruppierung
Die 1912 von Rainer Ludwig Claisen entdeckte Claisen-Umlagerung ist das erste aufgezeichnete Beispiel einer [3,3]-sigmatropen Umlagerung. Diese Umlagerung ist eine nützliche Kohlenstoff-Kohlenstoff-Bindungs-Bildungsreaktion. Ein Beispiel für die Claisen-Umlagerung ist die [3,3]-Umlagerung eines Allylvinylethers, die beim Erhitzen ein γ,γ-ungesättigtes Carbonyl ergibt. Die Bildung einer Carbonylgruppe macht diese Reaktion im Gegensatz zu anderen sigmatropen Umlagerungen von Natur aus irreversibel.

Aromatische Claisen-Umordnung
Die ortho-Claisen-Umlagerung beinhaltet die [3,3]-Verschiebung eines Allylphenylethers zu einem Zwischenprodukt, das schnell zu einem ortho-substituierten Phenol tautomerisiert.
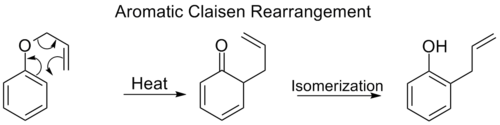
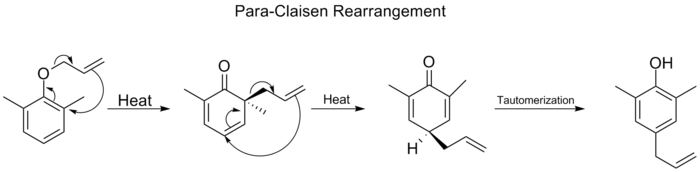
Wenn beide ortho-Positionen auf dem Benzolring blockiert sind, kommt es zu einer zweiten ortho-Claisen-Umlagerung. Diese Para-Claisen-Umlagerung endet mit der Tautomerisierung zu einem trisubstituierten Phenol.
Cope-Umlagerung
Das Cope-Rearrangement ist eine umfassend untersuchte organische Reaktion, bei der es sich um die [3,3] sigmatropische Umlagerung von 1,5-Dienen handelt. Sie wurde von Arthur C. Cope entwickelt. Zum Beispiel ergibt auf 300 °C erhitztes 3,4-Dimethyl-1,5-hexadien 2,6-Octadien.

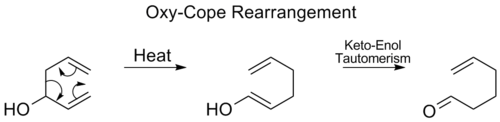
Oxy-Cope-Umlagerung
Bei der Oxy-Cope-Umlagerung wird bei C3 eine Hydroxylgruppe hinzugefügt, die nach der Keto-Enol-Tautomerie des intermediären Enols ein Enal oder Enon bildet:
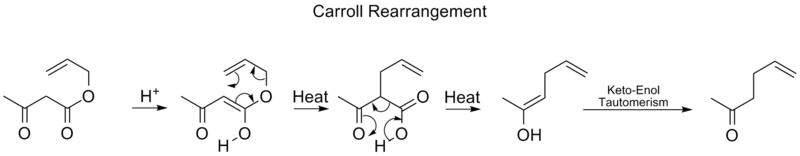
Neuordnung der Gehaltsliste
Die Carroll-Umlagerung ist eine Umlagerungsreaktion in der organischen Chemie und beinhaltet die Umwandlung eines β-Ketoallylesters in eine α-allyl-β-Ketocarbonsäure. Dieser organischen Reaktion kann eine Decarboxylierung folgen, und das Endprodukt ist ein γ,δ-Allylketon. Die Carroll-Umlagerung ist eine Anpassung der Claisen-Umlagerung und effektiv eine decarboxylierende Allylierung.
Fischer-Indol-Synthese
Die Fischer-Indolsynthese ist eine chemische Reaktion, bei der das aromatische heterocyclische Indol aus einem (substituierten) Phenylhydrazin und einem Aldehyd oder Keton unter sauren Bedingungen hergestellt wird. Die Reaktion wurde 1883 von Hermann Emil Fischer entdeckt.
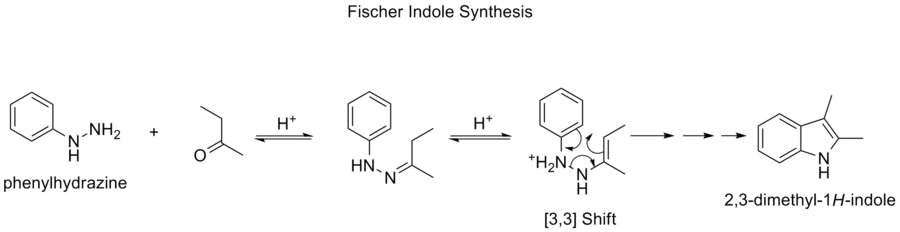
Die Wahl des Säurekatalysators ist sehr wichtig. Erfolgreiche Säurekatalysatoren umfassen: Brönsted-Säuren wie HCl, H2SO4, Polyphosphorsäure und p-Toluolsulfonsäure. Lewis-Säuren wie Bortrifluorid, Zinkchlorid, Eisenchlorid und Aluminiumchlorid sind ebenfalls nützliche Katalysatoren.
Es wurden mehrere Rezensionen veröffentlicht.
[5,5] Schichten
Ähnlich wie [3,3] Verschiebungen sagen die Woodward-Hoffman-Regeln voraus, dass [5,5] sigmatropische Verschiebungen suprafazial verlaufen würden, Huckel-Topologie-Übergangszustand. Diese Reaktionen sind seltener als [3,3]-sigmatrope Verschiebungen, aber dies ist hauptsächlich eine Funktion der Tatsache, dass Moleküle, die [5,5]-Verschiebungen durchlaufen können, seltener sind als Moleküle, die [3,3]-Verschiebungen durchlaufen können.
![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)
Umgruppierungen
Die Migration einer zweiwertigen Gruppe wie O, S, NR oder CR2, die Teil eines dreigliedrigen Rings in einem bicyclischen Molekül ist, wird gemeinhin als Gangumlagerung bezeichnet. Diese kann formal nach den Woodward-Hofmann-Regeln als eine (1, n) sigmatrope Verschiebung charakterisiert werden. Ein Beispiel für ein solches Rearrangement ist die Verschiebung von Substituenten auf Tropilidenen (1,3,5-Cycloheptatrienen). Bei Erwärmung durchläuft das pi-System einen elektrozyklischen Ring, der sich unter Bildung von bicycle[4,1,0]Heptadien (Norcaradien) schließt. Danach folgt eine [1,5]-Alkylverschiebung und eine elektrozyklische Ringöffnung.
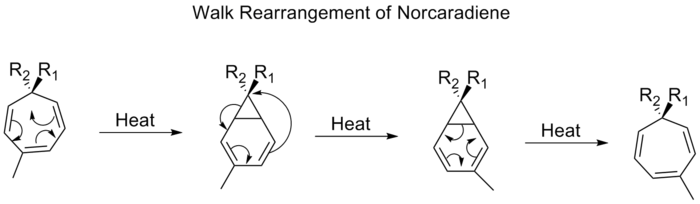
Es wird erwartet, dass die Gangumlagerung von Norcaradienen nach einer [1,5]-Verschiebung suprafazial verläuft und die Stereochemie erhalten bleibt. Experimentelle Beobachtungen zeigen jedoch, dass die 1,5-Verschiebungen der Norcaradiene antarafazial verlaufen. Theoretische Berechnungen ergaben, dass die [1,5]-Verschiebung ein diradikaler Prozess ist, der jedoch keine diradikalen Minima auf der Oberfläche der potentiellen Energie beinhaltet.
Verwandte Seiten
- 2,3-sigmatropische Umlagerung
- NIH-Verschiebung
- Grenzüberschreitende molekulare Orbital-Theorie
- Woodward-Hoffmann-Regeln
Fragen und Antworten
F: Was ist eine sigmatrope Reaktion in der organischen Chemie?
A: Eine sigmatrope Reaktion ist eine perizyklische Reaktion, die einen unkatalysierten intramolekularen Prozess beinhaltet und eine σ-Bindung in eine andere σ-Bindung umwandelt.
F: Ist bei einer sigmatropen Reaktion ein Katalysator erforderlich?
A: Für eine sigmatrope Reaktion ist in der Regel kein Katalysator erforderlich, obwohl einige sigmatrope Reaktionen durch eine Lewis-Säure katalysiert werden können.
Q: Was bedeutet der Begriff "sigmatrop"?
A: Der Begriff "sigmatrop" ist ein zusammengesetztes Wort aus "sigma", das sich auf einzelne Kohlenstoff-Kohlenstoff-Bindungen bezieht, und dem griechischen Wort "tropos", das "drehen" bedeutet.
F: Welche Art von Reaktion ist eine sigmatrope Reaktion?
A: Eine sigmatrope Reaktion ist eine Umlagerungsreaktion, d.h. die Bindungen in einem Molekül verschieben sich zwischen den Atomen, ohne dass Atome das Molekül verlassen oder neue Atome hinzugefügt werden.
Q: Was geschieht bei einer intramolekularen sigmatropen Reaktion?
A: Bei einer intramolekularen sigmatropen Reaktion bewegt sich ein Substituent von einem Teil eines π-gebundenen Systems zu einem anderen Teil mit gleichzeitiger Umordnung des π-Systems.
F: Gibt es bekannte sigmatrope Umlagerungen?
A: Einige der bekanntesten sigmatropen Umlagerungen sind die [3,3] Cope-Umlagerung, die Claisen-Umlagerung, die Carroll-Umlagerung und die Fischer-Indol-Synthese.
F: Sind an sigmatropen Reaktionen häufig Übergangsmetallkatalysatoren beteiligt?
A: Ja, an sigmatropen Reaktionen sind oft Übergangsmetallkatalysatoren beteiligt, die in analogen Reaktionen Zwischenstufen bilden.