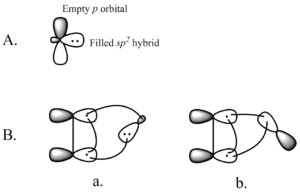
Cheletropische Reaktionen sind eine spezielle Klasse pericyclischer Prozesse, bei denen in einem einzigen Schritt zwei Bindungen zu demselben Atom gebildet oder gebrochen werden. Als pericyclische Reaktion zeichnen sie sich durch einen azyklischen oder zyklischen Übergangszustand mit einer konzertierten Umlagerung von σ- und π-Bindungen aus. In Konsequenz sind stereochemische Konsequenzen und Orbitalsymmetrie oft entscheidend für Verlauf und Selektivität.
Charakteristische Merkmale
Typisch für cheletropische Reaktionen ist, dass beide neuen Bindungen an einem einzigen Atom entstehen (cheleto-: "Klaue"). Man unterscheidet allgemein cheletropische Additionen, bei denen ein kleines Molekül an eine Mehrfachbindung addiert, und cheletropische Extrusionen, bei denen ein kleines Molekül abgespalten wird. Die Vorgänge lassen sich in den Kontext der allgemeinen Theorie pericyclischer Reaktionen einordnen, etwa durch Betrachtung der pericyclischen Übergangszustände und der Erhaltung der Orbitalsymmetrie nach Woodward–Hoffmann-ähnlichen Prinzipien.
Mechanismus und Steuerfaktoren
Mechanistisch verlaufen cheletropische Reaktionen meist concerted, das heißt ohne isolierbare Zwischenstufen. Entscheidend sind die Phasenbeziehungen der beteiligten π- und σ-Orbitale: deren Wechselwirkung bestimmt, ob ein bestimmter Annäherungsmodus energetisch zugänglich ist. Neben elektronischen Effekten beeinflussen sterische Hinderung, Temperatur und die mögliche Freisetzung eines Gases die Reaktionsrate und Lage des Gleichgewichts. Häufig ist die Entropieeinheit durch Gasfreisetzung (z. B. CO oder N2) eine treibende Kraft für Extrusionen.
Typische Beispiele und Anwendungen
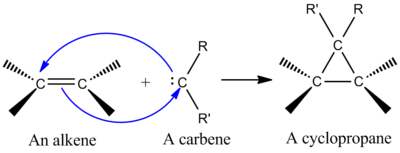
- Cyclopropanierung von Alkenen durch Carbenes: Das Carbene bildet zwei neue Bindungen an dasselbe Kohlenstoffatom bzw. an die beiden Doppelbindungsatome; dies ist ein klassisches cheletropisches Additionsbeispiel.
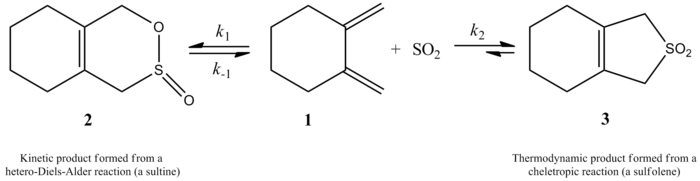
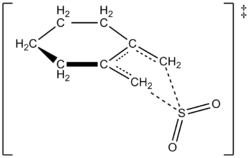
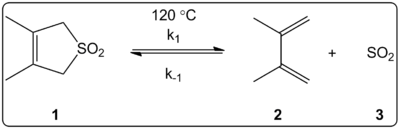
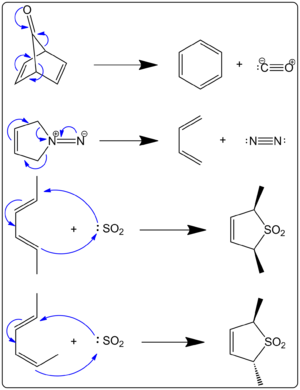
- Addition von SO2 an konjugierte Diene zur Bildung von Sulfolenen — eine synthetisch nützliche Methode zur Einbindung von Schwefeldioxid.
- Extrusion kleiner Moleküle (CO, N2) aus Vorstufen: solche cheletropischen Extrusionen werden in der organischen Synthese und in der Koordinationschemie beobachtet, wobei die Freisetzung eines Gases den Prozess begünstigen kann.
- Modellreaktionen in der Methodenentwicklung: cheletropische Schritte dienen oft dazu, kleine Ringe zu bilden oder funktionelle Gruppen gezielt einzuführen.
Bedeutung für Forschung und Synthese
Cheletropische Reaktionen sind für die organische Synthese wichtig, weil sie in einem einzigen Schritt differenzierte strukturelle Veränderungen erlauben. Sie werden sowohl in der akademischen Mechanistik (kinetische und spektroskopische Untersuchungen, isotopenmarkierte Studien) als auch in der praktischen Anwendungen zur Herstellung von zyklischen Bausteinen eingesetzt. Reaktionen dieser Klasse werden durch kinetische und thermodynamische Messungen sowie durch computergestützte Berechnungen untersucht.
Abgrenzung und Hinweise
Wichtig ist die Abgrenzung zu anderen pericyclischen Prozessen: Während bei normalen Cycloadditionen zwei Bindungen an unterschiedlichen Atomen entstehen, konzentriert sich die cheletropische Variante auf ein gemeinsames Atom. Praktisch lassen sich cheletropische Reaktionen durch stereospezifische Produkte, die beobachtete Gasfreisetzung und durch charakteristische kinetische Gesetzmäßigkeiten identifizieren. Instrumentelle Methoden wie NMR, IR und Massenspektrometrie sowie Vergleich mit Modellrechnungen helfen, cheletropische Mechanismen zu bestätigen.
Für weiterführende Hintergrundinformationen siehe: Grundlagen pericyclischer Reaktionen, Beispiele in der Synthese und Übersichtsartikel zu cheletropischen Extrusionen. Ergänzende Lehrbücher und Reviews besprechen experimentelle Techniken und theoretische Deutungen; eine Einführung bietet auch die Betrachtung der Orbitalwechselwirkung-Prinzipien.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)