Das Pflaumenpuddingmodell war ein frühes (und falsches) Atommodell des 20. Jahrhunderts. Es wurde von J.J. Thomson 1904, nach der Entdeckung des Elektrons, aber vor der Entdeckung des Atomkerns, vorgeschlagen. Zu dieser Zeit wussten die Wissenschaftler, dass es im Atom eine positive Ladung gab, die die negativen Ladungen der Elektronen ausglich und das Atom neutral machte, aber sie wussten nicht, woher die positive Ladung stammte. Thomsons Modell zeigte ein Atom, das ein positiv geladenes Medium oder einen positiv geladenen Raum mit negativ geladenen Elektronen im Inneren des Mediums hatte. Bald nach seinem Vorschlag wurde das Modell als "Pflaumenpudding"-Modell bezeichnet, weil das positive Medium wie ein Pudding war, mit Elektronen oder Pflaumen im Inneren.
Thomsonsches Atommodell
Entwicklung zum modernen Atommodell
Rutherfords Modell
Im Grunde machten Hans Geiger und Ernest Marsden 1909, nicht lange nachdem Thomsons Modell vorgeschlagen wurde, ein Experiment mit dünnen Goldblechen, um Thomsons Modell zu testen. Ihr Professor, Ernest Rutherford, erwartete, dass die Ergebnisse Thomson Recht geben würden, aber ihre Ergebnisse wichen extrem von dem ab, was sie erwartet hatten. Im Jahr 1911 entdeckte Rutherford, dass die positiven Ladungen von winzigen Teilchen, den Protonen, stammen und dass die Protonen sich in einem winzigen Zentrum, dem Kern, befinden und dass die Elektronen um den Kern kreisen.
Modell Bohr
Rutherfords Modell war recht einfach, aber es war falsch, denn Elektronen haben Ladung, und sie sollten von dem positiv geladenen Kern angezogen werden. 1913 fügte Niels Bohr dem Atommodell "Energieniveaus" hinzu. Elektronen fallen nicht in den Kern, weil sie in Energieniveaus enthalten sind, und um zu höheren Energieniveaus zu wechseln, ist zusätzliche Energie erforderlich, und um zu niedrigeren Energieniveaus zu wechseln, ist eine Energiefreisetzung erforderlich. Es ist nicht möglich, Energiezustände zu ändern, ohne die Energie des Elektrons zu verändern. Wenn ein Elektron von einem Photon (einem Teilchen, das elektromagnetische Strahlung trägt) getroffen wird, gewinnt es zusätzliche Energie und geht in ein höheres Energieniveau über (es ändert seine Zustände), dann springt es zurück auf ein niedrigeres Energieniveau und gibt seine enthaltene Energie frei. Dieses neue Modell wurde das Bohr-Modell oder das Rutherford-Bohr-Modell genannt. Damit wurde ein ganz neuer Zweig der Wissenschaft hinzugefügt: die Quantenphysik.
Quanten-Modell
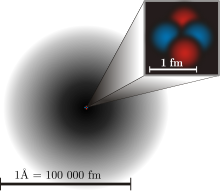
1926 benutzte Erwin Schrödinger die Idee, dass Elektronen nicht nur als Teilchen, sondern auch als Welle agieren, dies wird als Welle-Teilchen-Dualismus bezeichnet. Damit wurde dem Atommodell und der Quantenphysik eine ganz neue Schicht hinzugefügt. Bei einem Teilchen kann man wissen, wo es sich im Raum befindet, wenn man es beobachtet (anschaut). Aber bei einer Welle ist es überall, so dass man nicht genau definieren kann, wo es sich befindet. Dies ist als Quantenunsicherheit bekannt. Bei einem Elektron kann man nur die Wahrscheinlichkeit kennen, dass es sich an einem Ort befindet, denn es ist sowohl eine Welle als auch ein Teilchen. (Siehe Diagramm oben)


Verwandte Seiten
- Atomtheorie
- Quantenmechanik
- J. J. Thomson
- Ernest Rutherford
- Niels Bohr
- Erwin Schrödinger
