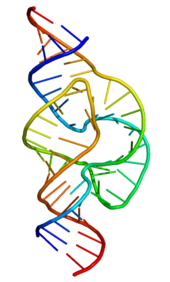
Ein Ribozym (Ribonukleinsäure-Enzym) ist ein RNA‑Molekül, das bestimmte biochemische Reaktionen katalysieren kann, ähnlich der Wirkung von Protein‑Enzymen. Anders als passive Informationsspeicher kann katalytische RNA durch ihre spezifische Faltung chemische Bindungen spalten, verknüpfen oder umlagern und so als biologischer Katalysator wirken.
Funktion und Wirkungsweise
Ribozyme beschleunigen Reaktionen, indem sie eine geeignete dreidimensionale Struktur ausbilden, die Reaktanden präzise anordnet. Typische Mechanismen umfassen:
- Stabilisierung von Übergangszuständen durch spezifische Basenpaarungen und tertiäre Wechselwirkungen,
- General‑acid/base‑Katalyse durch aktive Nukleotide,
- Koordination von Metallionen (z. B. Mg2+), die als Katalysatoren fungieren und die negative Ladung der Phosphodiesterbindungen abschirmen.
Im Ribosom übernimmt die ribosomale RNA (rRNA) beispielsweise die peptidyl‑transferase‑Aktivität: Das heißt, die eigentliche Verknüpfung von Aminosäuren während der Proteinsynthese wird nicht von einem Protein, sondern von RNA katalysiert. Weitere natürliche Funktionen von Ribozyms umfassen das RNA‑Spleißen, die Reifung von tRNA‑ Vorstufen (RNase P) sowie die Selbst‑Spaltung oder -Ligierung in einigen Viren und mobilen Elementen.
Wichtige Typen natürlicher Ribozyme
- RNase P: Ein ribonukleoprotein, dessen RNA‑Anteil die eigentliche Endonuklease‑Aktivität trägt und Vorläufer‑tRNA an der richtigen Stelle schneidet.
- Group‑I und Group‑II Introns: Selbstspleißende RNA‑Elemente, die ihre eigenen Introns entfernen können; Group‑II‑Introns gelten als mögliches Vorbild für das heutige Splicing‑Apparat der Eukaryoten.
- Hammerhead, Hairpin, Hepatitis‑Delta (HDV)‑Ribozyme: Kleine, selbstspaltende Motive, die oft in Viren oder Satellitenelementen vorkommen.
- glmS‑Ribozyme: Ein metabolitabhängiges Ribozym, das als riboswitch fungiert und seine Aktivität durch Bindung eines Metaboliten reguliert.
Bedeutung für die RNA‑Welt‑Hypothese
Die Entdeckung katalytischer RNA Anfang der 1980er Jahre veränderte unser Verständnis von Biochemie: RNA kann sowohl genetische Information tragen als auch chemische Reaktionen katalysieren. Diese Doppelfunktion ist die Basis der RNA-Welthypothese, welche annimmt, dass in frühen Stadien der chemischen Evolution RNA eine zentrale Rolle bei der Speicherung von Information und bei katalytischen Prozessen spielte. Solche Eigenschaften hätten die Entstehung selbstreplizierender, präbiotischer Systeme ermöglicht.
Ribozyme im Labor und synthetische Varianten
In vitro‑Methoden wie die selektive Evolution (z. B. SELEX) haben es ermöglicht, Ribozyme mit neuen oder verbesserten Aktivitäten zu züchten. Forscher, die den Ursprung des Lebens untersuchen, haben im Labor Ribozyme entwickelt, die unter definierten Bedingungen RNA‑ Polymerase‑Aktivität zeigen und so die Synthese von RNA‑Strängen katalysieren können. Beispiele aus der experimentellen Evolution sind Varianten wie das "Rund‑18"‑Polymerase‑Ribozym, die weiterentwickelte Versionen B6.61 und das Ribozym "tC19Z". B6.61 kann innerhalb von 24 Stunden bis zu etwa 20 Nukleotide an einen Primer‑Template‑Komplex anfügen, bevor es durch Spaltung seiner Phosphodiesterbindungen zerfällt. Das Ribozym "tC19Z" gelangt bis zu ~95 Nukleotide mit hoher Genauigkeit.
Solche Ergebnisse zeigen das Potential der RNA‑Katalyse, sind aber noch weit von einer vollständig autonomen, langlebigen Selbstreplikation entfernt; Stabilität, Fehleranfälligkeit und Ausdauer sind weiterhin limitierende Faktoren.
Anwendungen in Therapie, Diagnostik und Biotechnologie
Ribozyme werden als molekulare Werkzeuge und potenzielle Therapeutika erforscht. Mögliche Einsatzgebiete sind:
- Therapeutische Ribozyme, die gezielt krankheitsrelevante RNA‑Sequenzen spalten (experimentelle Ansätze gegen Viren wie HIV oder Hepatitis),
- Biosensoren: ribozyme oder riboswitchbasierte Systeme, die auf kleine Moleküle reagieren und ein messbares Signal erzeugen,
- Biotechnologische Anwendungen in der Genomik und Genforschung, etwa für RNA‑Modifikation, regulatorische Schaltkreise in der synthetischen Biologie oder als Bausteine für RNA‑basierte Nanostrukturen.
Herausforderungen für praktische Anwendungen sind vor allem die Stabilität in vivo (RNA‑Abbau durch RNasen), zielgerichtete Abgabe in Zellen und mögliche Immunreaktionen. Chemische Modifikationen der RNA und geeignete Lieferstrategien (Nanopartikel, Lipide) werden intensiv erforscht, um diese Probleme zu überwinden.
Forschung, Methoden und Ausblick
Methodisch kombinieren Forscher Strukturbiologie (Röntgenkristallographie, Kryo‑EM), biochemische Kinetik, Sequenzanalyse und gerichtete Evolution, um Strukturen, Mechanismen und Potenzial neuer Ribozyme zu entschlüsseln. Die weitere Entwicklung synthetischer Polymerase‑Ribozyme, besserer Liefervehikel und metabolitabhängiger Regelmechanismen könnte Ribozyme in Zukunft noch breiter nutzbar machen — sowohl als Werkzeug in der Grundlagenforschung als auch in medizinischen und technischen Anwendungen.
Insgesamt zeigen Ribozyme eindrücklich, dass RNA mehr kann als nur Information zu speichern: Sie ist ein vielseitiger, evolutionär bedeutsamer Katalysator mit großem Potenzial für Wissenschaft und Technik.