Es gibt Tausende von verschiedenen Enzymen, und jedes ist spezifisch für die Reaktion, die es katalysiert. Enzyme haben Namen, die zeigen, was sie tun. Die Namen von Enzymen enden gewöhnlich auf
-ase, um zu zeigen, dass es sich um Enzyme handelt. Beispiele hierfür sind die ATP-Synthase. Sie stellt eine Chemikalie namens
ATP her. Ein weiteres Beispiel ist die DNA-Polymerase. Sie liest einen intakten DNA-Strang und verwendet ihn als
Vorlage zur Herstellung eines neuen Stranges.
Ein Beispiel für ein Enzym ist die im Speichel vorkommende Amylase. Es spaltet Stärkemoleküle in kleinere Glukose- und Maltosemoleküle auf. Eine andere Art von Enzym ist die Lipase. Es spaltet Fette in kleinere Moleküle, Fettsäuren und Glycerin auf.
Die Proteasen sind eine ganze Klasse von Enzymen. Sie spalten andere Enzyme und Proteine wieder in Aminosäuren auf. Nukleasen sind Enzyme, die DNA oder RNA schneiden, oft an einer bestimmten Stelle im Molekül.
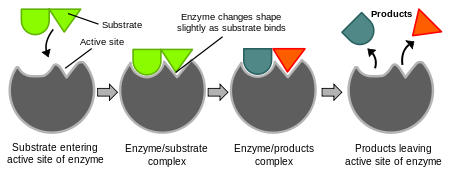
Enzyme dienen nicht nur dazu, große Chemikalien in kleinere Chemikalien aufzuspalten. Andere Enzyme nehmen kleinere Chemikalien und bauen sie zu größeren Chemikalien auf und erledigen viele andere chemische Aufgaben. Die nachstehende Klassifikation listet die Haupttypen auf.
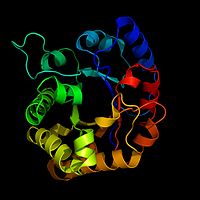
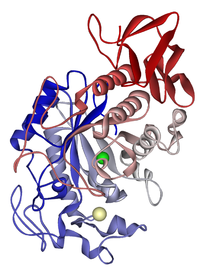
Biochemiker zeichnen oft ein Bild eines Enzyms, um es als visuelle Hilfe oder Karte des Enzyms zu verwenden. Das ist schwierig, da ein Enzym Hunderte oder Tausende von Atomen enthalten kann. Biochemiker können nicht all diese Details zeichnen. Stattdessen verwenden sie Bandmodelle als Bilder von Enzymen. Bandmodelle können die Form eines Enzyms zeigen, ohne jedes Atom zeichnen zu müssen.
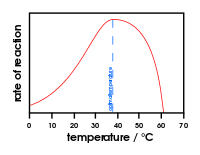
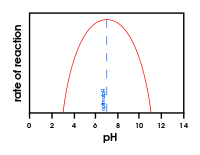
Die meisten Enzyme funktionieren nicht, wenn Temperatur und pH-Wert nicht genau richtig sind. Bei Säugetieren liegt die richtige Temperatur normalerweise bei etwa 37oC Grad (Körpertemperatur). Der richtige pH-Wert kann stark variieren. Pepsin ist ein Beispiel für ein Enzym, das am besten funktioniert, wenn der pH-Wert etwa 1,5 beträgt.
Wenn ein Enzym über eine bestimmte Temperatur erhitzt wird, wird das Enzym dauerhaft zerstört. Es wird durch Protease abgebaut und die Chemikalien werden wieder verwendet.
Einige Chemikalien können einem Enzym helfen, seine Arbeit noch besser zu tun. Diese werden Aktivatoren genannt. Manchmal kann eine Chemikalie ein Enzym verlangsamen oder sogar dazu führen, dass das Enzym überhaupt nicht mehr arbeitet. Diese werden als Inhibitoren bezeichnet. Die meisten Medikamente sind Chemikalien, die ein Enzym im menschlichen Körper entweder beschleunigen oder verlangsamen.