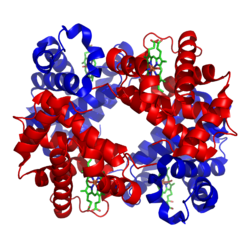
Hämoglobin (Kurzform: Hb) ist ein eisenhaltiges Protein in den roten Blutkörperchen, dessen wichtigste Aufgabe der Transport von Sauerstoff im Körper ist. Hämoglobin kommt in den roten Blutkörperchen nahezu aller Wirbeltiere vor (Ausnahme: einige weißblütige Fische) und ist außerdem in bestimmten wirbellosen Tieren vorhanden. Andere wirbellose Tiere nutzen stattdessen andere Atemproteine, z. B. Hämocyanin. Das in Hämoglobin gebundene Eisen (Eisen) verleiht dem Blut seine rote Farbe. Ist an Hämoglobin Sauerstoff gebunden, spricht man von Oxyhämoglobin.
Aufbau und Struktur
Hämoglobin ist ein Tetramer aus vier Globin-Untereinheiten (bei Erwachsenen meist zwei α- und zwei β-Ketten). Jede Untereinheit enthält eine Porphyrin-gebundene Häm-Gruppe mit einem zentralen Eisenion (Fe2+), das den Sauerstoff reversibel binden kann. Unterschiedliche Globin-Ketten entstehen durch unterschiedliche Gene; so gibt es bei Menschen verschiedene Hämoglobin-Typen (z. B. HbA, HbA2, HbF).
Funktion und Sauerstofftransport
Die Hauptfunktion von Hämoglobin ist der bidirektionale Transport von Sauerstoff von der Lunge zu den Geweben und die Rückführung von Kohlendioxid bzw. Protonen in die Lunge. In der Lunge bindet Hämoglobin Sauerstoff und wird zu Oxyhämoglobin; in peripheren Geweben wird der Sauerstoff wieder freigesetzt und vom Zellstoffwechsel genutzt.
Allosterie, Kooperativität und der Sauerstoff-Dissoziationskurve
- Hämoglobin zeigt Kooperativität: die Bindung eines O2-Moleküls erhöht die Affinität der verbleibenden Bindungsstellen für O2. Das ergibt eine sigmoide Sauerstoff-Dissoziationskurve.
- Der P50-Wert (Druck, bei dem 50 % des Hämoglobins mit O2 gesättigt sind) liegt bei normalen Bedingungen bei etwa 26–27 mmHg; Verschiebungen der Kurve verändern die O2-Freisetzung.
- Wichtige Faktoren, die die Kurve verschieben:
- pH-Wert (Bohr-Effekt): niedrigere pH-Werte (mehr H+) verringern die O2-Affinität und fördern die Freisetzung.
- pCO2: höherer CO2-Partialdruck fördert O2-Abgabe.
- Temperatur: erhöhte Temperatur reduziert die Affinität für O2.
- 2,3-Bisphosphoglycerat (2,3-BPG): erhöht die O2-Freisetzung im Gewebe.
Rolle beim Transport anderer Gase
Hämoglobin bindet nicht nur Sauerstoff, sondern ist auch am Transport von Kohlendioxid beteiligt: etwa 20–25 % des im Blut transportierten Kohlendioxids der Atemwege ist an Hämoglobin gebunden (als Carbamino-Verbindung oder durch pH-abhängigen Austausch) – zusätzlich wird CO2 größtenteils in Form von Bicarbonat im Plasma transportiert.
Spezielle Bindungen und Störungen
- CO (Kohlenmonoxid) bindet mit deutlich höherer Affinität an das Häm-Eisen als O2 und kann so die Sauerstoffaufnahme blockieren (CO-Vergiftung).
- Methemoglobin entsteht, wenn Eisen im Häm zu Fe3+ oxidiert; Met-Hb kann keinen O2 mehr binden und führt zu funktioneller Hypoxie.
- Genetische Erkrankungen wie Sichelzellanämie (Punktmutation in der β-Kette) oder Thalassämien (verminderte Produktion von Globin-Ketten) beeinträchtigen Struktur oder Menge des Hämoglobins und verursachen Anämie bzw. weitere Komplikationen.
Biologische Aspekte: Synthese, Lebensdauer und Recycling
Hämoglobin wird in den Vorläuferzellen der Erythrozyten synthetisiert. Rote Blutkörperchen haben eine Lebensdauer von circa 120 Tagen; beim Abbau in Milz und Leber wird das Eisen aus dem Häm recycelt und für neue Erythrozyten verwendet. Störungen in der Synthese oder im Recycling können zu Eisenmangel oder Eisenüberladung führen.
Klinische Bedeutung und Messung
Der Hämoglobinwert im Blut ist ein zentraler Laborparameter zur Beurteilung des Sauerstofftransportpotenzials und zur Diagnose von Anämien. Übliche Referenzbereiche (können je nach Labor und Population leicht variieren):
- Männer: ca. 13,8–17,2 g/dL
- Frauen: ca. 12,1–15,1 g/dL
Weitere klinisch relevante Tests umfassen die Bestimmung von:
- Hämoglobinspezies (z. B. Oxyhämoglobin, Carboxyhämoglobin, Methemoglobin)
- Hämatokrit und Erythrozytenzahl
- Blutgasanalyse zur Bestimmung von pO2, pCO2 und Säure-Basen-Status
Zusammenfassung
Hämoglobin ist ein zentrales Transportprotein im Blut: es bindet reversibel Sauerstoff, unterstützt den CO2-Transport und wird fein durch pH, CO2, Temperatur und 2,3-BPG reguliert. Strukturveränderungen oder Störungen in Menge bzw. Funktion des Hämoglobins führen zu klinisch relevanten Erkrankungen, die häufig diagnostisch über den Hämoglobinwert und weiterführende Laboruntersuchungen erfasst werden.