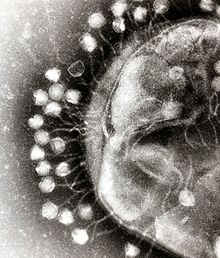
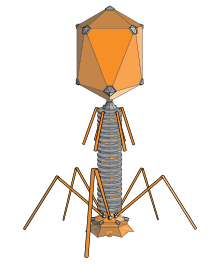
Ein Bakteriophage ist ein Virus, der Bakterien infiziert. Der Begriff wird häufig kurz als Phage bezeichnet. Phagen sind keine Einzeller, sondern obligat intrazelluläre Parasiten: sie benötigen lebende Wirtsbakterien, um ihr Genom zu vermehren und neue Virionen zu produzieren.
Aufbau und genetische Vielfalt
Phagen bestehen typischerweise aus einer Proteinhülle (Kapsid), die das genetische Material umschließt. Das Genom kann aus einzelsträngiger (ssRNA oder ssDNA) oder doppelsträngiger (dsRNA oder dsDNA) Nukleinsäure bestehen, ist zwischen etwa 5 und 500 Kilobasenpaare lang und kann linear oder zirkulär angeordnet sein. Die physikalische Größe vieler Phagen liegt im Bereich von etwa 20 bis 200 Nanometer.
Phagengenome kodieren nur eine kleine Anzahl essentieller Funktionen (manche wenige, andere mehrere hundert Gene) und werden sehr effizient genutzt. Strukturell unterscheiden sich Phagen stark: viele besitzen ein ikosaedrisches Kapsid und einen Schwanz, andere sind filamentös oder haben komplexe Formen. Klassifikatorisch gehören zahlreiche Phagenfamilien zu den am stärksten diversifizierten Virengruppen.
Lebenszyklus: lytisch und lysogen
Phagen können zwei grundsätzliche Lebensstrategien verfolgen:
- Lytischer Zyklus: Der Phage bindet an die Bakterienoberfläche, injiziert sein Genom, übernimmt den Stoffwechsel des Wirts, repliziert sein Erbgut, baut neue Kapside und setzt die neuen Virionen durch Lyse (Auflösung) der Wirtszelle frei.
- Lysogener Zyklus: Das Phagengenom integriert sich in das Bakterienchromosom oder bleibt als stabile, nicht replikative Form im Zellinneren (Prophage). Der Wirtsstamm vermehrt sich zunächst normal. Unter bestimmten Bedingungen kann der Prophage aktiviert werden (Induktion) und in den lytischen Zyklus übergehen.
Durch diese Wechselwirkung beeinflussen Phagen die Genetik ihrer Wirte, unter anderem durch horizontale Gentransfermechanismen wie Transduktion.
Vorkommen und ökologische Bedeutung
Phagen sind nahezu überall dort zu finden, wo Bakterien vorkommen — im Boden, in der Tierdarmflora, in Süß- und Meerwasser sowie in technischen Systemen wie Kläranlagen. Im Meer sind sie besonders zahlreich: in mikrobiellen Matten an der Oberfläche wurden bis zu 9×10^8 Virionen pro Milliliter gemessen, und Schätzungen zufolge können bis zu 70% der Meeresbakterien durch Phagen infiziert sein.
Ökologisch steuern Phagen Bakterienpopulationen, beeinflussen biogeochemische Kreisläufe (z. B. Kohlenstoff- und Nährstofffreisetzung) und tragen zur Diversität mikrobieller Gemeinschaften bei, indem sie selektiv Wirtsstämme dezimieren.
Phagen und Biofilme
Biofilme sind bakterielle Gemeinschaften, die in einer schützenden Matrix eingebettet sind. Die Beziehung zwischen Phagen und Biofilmen ist komplex: einige Phagen produzieren Enzyme (z. B. Polysaccharid‑Depolymerasen), die Biofilmmatrizen auflösen und so Bakterien zugänglicher machen; andere Phagen (insbesondere temperente Phagen) können durch Integration in Wirtsgene zur Stabilisierung oder Verstärkung von Biofilmen beitragen. In bestimmten Krankheitsverläufen — etwa bei Lungenentzündung oder Mukoviszidose — beeinflussen Phagen die Empfindlichkeit von Biofilmen gegenüber Antibiotika und damit den Verlauf der Infektion.
Phagen in der Therapie (Phagen‑Therapie)
Die Nutzung von Phagen zur Bekämpfung bakterieller Infektionen hat eine lange Geschichte: in Teilen der ehemaligen Sowjetunion, in Mitteleuropa und in Frankreich als Alternative zu Antibiotika werden Phagen seit Jahrzehnten angewandt. Nachdem bereits 1939 Helmut Ruska erste Phagen im Elektronenmikroskop beobachtet hatte, rückte ihre Natur stärker ins wissenschaftliche Bewusstsein. In den letzten Jahren erlebt die Phagenforschung wegen zunehmender antibiotikaresistenter Erreger ein weltweites Comeback.
Mögliche Vorteile der Phagen‑Therapie:
- Hohe Spezifität gegenüber Zielbakterien — schonende Wirkung auf die normale Flora.
- Selbstverstärkung am Infektionsort: Phagen vermehren sich so lange, wie empfindliche Wirte vorhanden sind.
- Potential zur Auflösung von Biofilmen durch phagen‑kodierte Enzyme.
Herausforderungen und Risiken:
- Enge Wirtsspezifität erfordert genaue Identifikation des Erregers oder die Verwendung von Phagen‑Cocktails.
- Immunsystemreaktionen können Phagen neutralisieren.
- Gefahr des horizontalen Gentransfers (z. B. Übertragung von Resistenz- oder Virulenzgenen) — sorgfältige Charakterisierung ist notwendig.
- Regulatorische, herstellungstechnische und Qualitäts‑/Sicherheitsanforderungen sind komplex und werden weltweit noch entwickelt.
Es gibt mittlerweile dokumentierte Einzelfälle und erste klinische Studien, die erfolgreiche Anwendungen von Phagen bei sonst therapieresistenten Infektionen berichten. Dennoch sind weitere kontrollierte Studien nötig, um Wirksamkeit, Dosierung, Therapiekombinationen und Langzeitsicherheit umfassend zu belegen.
Forschung, Produktion und Zulassung
Für eine sichere Anwendung müssen Phagen isoliert, sequenziert und auf mögliche unerwünschte Gene (z. B. Toxine, Resistenzgene) geprüft werden. Die Herstellung erfordert Reinheitskontrollen (Entfernung bakterieller Bestandteile und Endotoxine) und standardisierte Formulierungen. In einigen Ländern existieren spezialisierte Phagenbanken und institutionelle Programme für compassionate use; internationale Regelwerke zur Zulassung von Phagenpräparaten stehen noch am Anfang.
Schlussbemerkung
Bakteriophagen gehören zu den häufigsten und vielfältigsten Entitäten der Biosphäre. Sie sind sowohl ökologische Schlüsselspieler als auch vielversprechende Instrumente im Kampf gegen antibiotikaresistente Bakterien. Gleichzeitig erfordern ihre Nutzung in der Medizin und Industrie fundierte Forschung, stringente Sicherheitsprüfungen und abgestimmte regulatorische Rahmenbedingungen, damit Potenziale sicher und effektiv genutzt werden können.