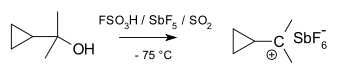
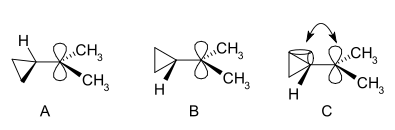
Ein Carbokation ist ein Ion, bei dem ein Kohlenstoffatom positiv geladen ist. Carbokationen spielen eine zentrale Rolle in vielen organischen Reaktionen und gelten als reaktive Zwischenstufen.
Elektronische Struktur
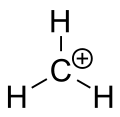
Das positiv geladene Kohlenstoffatom besitzt nur ein Sextett statt der gewohnten acht Valenzelektronen: es hat nur sechs Elektronen in seiner äußeren Valenzschale. Dies widerspricht der Oktett-Regel und erklärt, warum Carbokationen oft energetisch ungünstig sind und hohe Reaktionsfreudigkeit zeigen. Viele Eigenschaften von Carbokationen lassen sich durch folgende Konzepte beschreiben:
- Hybridisierung: In klassischen Beschreibungen würde ein Carbokation eine sp3-Hybridisierung mit einem leeren sp3-Orbital besitzen; experimentelle und theoretische Befunde sprechen jedoch meist für eine sp2-Hybridisierung mit einem leeren p-Orbital.
- Geometrie: Das positiv geladene Zentrum ist häufig trigonal planar; die Molekülgeometrie entspricht daher meistens einer ebenen Anordnung der drei Substituenten um das Kohlenstoffzentrum.
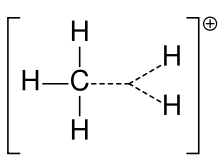
- Ladungsverteilung: Die positive Ladung ist nicht immer lokal am Kohlenstoff, sondern kann durch Hyperkonjugation und Resonanz über benachbarte Atome verteilt werden.
Klassifikation und Stabilität
Carbokationen werden nach der Stellung des geladenen Kohlenstoffatoms klassifiziert. Wichtige Typen sind:
- Methyl‑Carbokation (–CH3+)
- Primäres Carbokation (ein benachbarter Alkylrest)
- Sekundäres Carbokation (zwei Alkylreste)
- Tertiäres Carbokation (drei Alkylreste)
- Allylische und benzylische Carbokationen (stark resonanzgestützt)
- Nicht‑klassische bzw. bridged Carbokationen (Ladung delokalisiert über mehrere Bindungen)
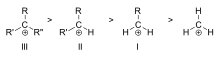
Allgemein gilt: tertiär > sekundär > primär > methyl hinsichtlich der thermodynamischen Stabilität, wobei zusätzliche Effekte wie Resonanzstabilisierung oder elektronische Substituenten die Reihenfolge beeinflussen können.
Stabilisierende Einflüsse
- Hyperkonjugation: σ‑Bindungen benachbarter C–H oder C–C‑Bindungen können Elektronendichte in das leere Orbital verschieben und so stabilisieren.
- Resonanz: Benzyliche und allylische Carbokationen sind durch Delokalisierung der Ladung über ein π‑System deutlich stabiler.
- Induktive Effekte: Elektronenschiebende Substituenten erhöhen die Stabilität, elektronenziehende Substituenten verringern sie.
Bildung und typische Reaktionen
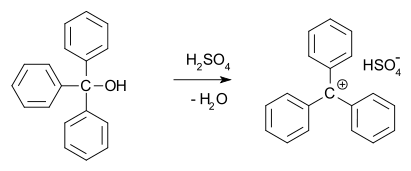
Carbokationen entstehen unter verschiedenen Bedingungen und sind Zwischenstufen zahlreicher Reaktionen:
- Ionisation (z. B. SN1‑Mechanismus bei der Abspaltung einer Abgangsgruppe)
- Protonierung von Alkenen oder anderen π‑Systemen
- Hydrid‑ oder Alkyl‑Abstraktion durch starke Elektrophile
- Solvolyse oder Säurekatalyse
Häufige Reaktionen, an denen Carbokationen beteiligt sind:
- Nukleophile Addition an das positiv geladene Kohlenstoffzentrum
- Rearrangements (z. B. Hydrid‑ oder Methylwanderung), die zu stabileren Carbokationen führen können
- Eliminierungen (zur Bildung von Alkenen)
- Additionen an Doppelbindungen unter Säurekatalyse
Die generelle Reaktivität von Carbokationen macht sie zu Schlüsselzwischenschritten in vielen synthetischen Verfahren.
Nachweis und praktische Bedeutung
- Direkter Nachweis gelingt in seltenen Fällen durch tiefgekühlte (low‑temperature) NMR‑Spektren oder in supersauren Medien, in denen Carbokationen ausreichend stabil sind.
- In der organischen Synthese werden Kenntnisse über Carbokationen genutzt, um Reaktionswege zu steuern oder unerwünschte Umlagerungen zu vermeiden.
- Die Vorstellung des Carbokations als planar‑hybridisiertes Zentrum mit leerem p‑Orbital ist ein hilfreiches Modell zur Vorhersage von Produktverteilungen.