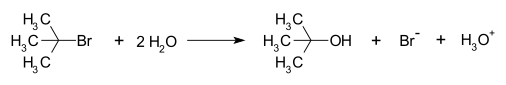
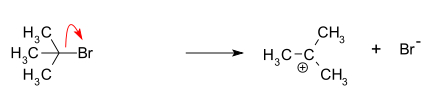
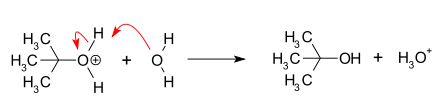
Die SN1-Reaktion ist eine Substitutionsreaktion in der organischen Chemie. "SN" steht für nukleophile Substitution und die "1" repräsentiert die Tatsache, dass der geschwindigkeitsbestimmende Schritt nur ein Molekül (unimolekular) betrifft. Charakteristisch für den Mechanismus ist die Bildung eines Carbokations-Zwischenprodukts. Typischerweise verlaufen SN1-Reaktionen an sekundären oder tertiären Alkylhalogeniden oder an stabilisierten Systemen (z. B. benzylich, allylisch) in polaren, protischen Lösungsmitteln oder unter sauren Bedingungen; primäre Alkylhalogenide reagieren dagegen meist über die alternative SN2-Reaktion. Unter anorganischen Chemikern wird die SN1-Reaktion oft als dissoziativer Mechanismus bezeichnet. Christopher Ingold et al. schlugen den Reaktionsmechanismus erstmals 1940 vor.
Mechanismus (Schritt-für-Schritt)
- 1. Bildung des Carbokations (geschwindigkeitsbestimmender Schritt): Das Substrat R–LG (R = Alkylrest, LG = Abgangsgruppe) spaltet die Abgangsgruppe ab und bildet ein Carbokation R+ sowie das Anion LG−. Dieser Schritt ist energetisch am aufwendigsten und bestimmt die Reaktionsgeschwindigkeit.
- 2. Angriff des Nukleophils: Ein Nukleophil N: greift das elektrophile Carbokation an und bildet das Produkt R–N. Dieser Schritt verläuft meist schnell.
- 3. Gegebenenfalls Deprotonierung oder Solvolyse: Bei Solvensnukleophilen (z. B. H2O, ROH) kann zunächst ein protoniertes Zwischenprodukt entstehen, das dann deprotoniert wird.
Kinetik
SN1-Reaktionen folgen einer ersten Ordnung im Substrat: rate = k [R–LG]. Die Geschwindigkeit ist unabhängig von der Konzentration des Nukleophils, da dessen Angriff nicht der geschwindigkeitsbestimmende Schritt ist.
Faktoren, die die SN1-Reaktion begünstigen
- Substratstruktur: Stabilität des Carbokations ist entscheidend. Tertiäre Carbokationen >> sekundäre > primäre. Stabilisierende Effekte durch Benzylicität, Allylizität oder Resonanz erhöhen die Neigung zur SN1.
- Abgangsgruppe: Gute Abgangsgruppen (z. B. I−, Br−, Tosylat) erleichtern die Ionisation.
- Solvens: Polare, protische Lösungsmittel (z. B. H2O, Alkohole) stabilisieren Ionen und fördern SN1. Aprotic solvents begünstigen eher SN2.
- Nukleophilie: Für die Geschwindigkeitsbestimmung unerheblich, aber ein sehr schwaches Nukleophil (z. B. Lösungsmittel selbst) begünstigt oft den SN1-Weg.
- Temperatur/Polarität: Höhere Temperaturen und eine hohe Dielektrizitätskonstante des Lösungsmittels begünstigen die Ionisation.
Stereochemie und Ion-Paar-Effekte
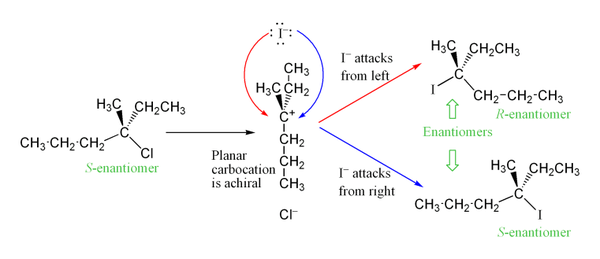
Beim Angriff auf ein planar aufgebautes Carbokation erwartet man Racemisierung, wenn das stereogene Zentrum betroffen ist. In der Praxis beobachtet man oft nur teilweise Racemisierung, weil das Gegenion (LG−) oder Solventmoleküle eine ionische Paarung oder eine solvent-separated ion pair bilden können; dadurch kann ein teilweiser sterischer Schutz einer Seite des Carbokations verbleiben und zu einer gewissen Enantioselektivität führen.
Umlagerungen
Weil in SN1-Mechanismen Carbokationen als Zwischenstufen auftreten, sind Umlagerungen (Hydrid- oder Alkylverschiebungen) häufig. Solche Verschiebungen führen oft zu stabileren Carbokationen und damit zu unerwarteten Produkten, z. B. isomerisierten Alkoholen nach Hydrolyse.
Beispiele
- Hydrolyse von tert-Butylchlorid in Wasser: (CH3)3C–Cl → (CH3)3C+ + Cl− → (CH3)3C–OH (tert-Butanol).
- Solvolyse von benzylicen Halogeniden: Benzyliche Substrate reagieren besonders leicht über SN1, da das Benzylium-Kation durch Resonanz stabilisiert ist.
- Reaktionen von allylischen Halogeniden und von Substraten mit elektronenziehenden oder -donierenden Substituenten, die das Carbokation stabilisieren.
Vergleich SN1 vs. SN2 (kurz)
- SN1: Unimolekularer Geschwindigkeitsbestimmender Schritt, Carbokation-Zwischenstufe, bevorzugt tertiäre und resonanzstabilisierte Substrate, polare protische Lösungsmittel, mögliche Umlagerungen, Tendenz zur Racemisierung.
- SN2: Bimolekularer, konzertierter Übergangszustand mit nukleophilem Hintereingriff, bevorzugt primäre Substrate, weniger Umlagerungen, vollständige Inversion der Konfiguration.
Experimenteller Nachweis und Energieprofil
Experimentell lässt sich eine SN1-Reaktion durch erste Ordnung der Geschwindigkeitskonstante (Linearisierung: ln[c] gegen Zeit) nachweisen. Ein typisches Reaktionsenergiediagramm zeigt eine hohe Aktivierungsenergie für den Zerfall zum Carbokation (Übergangszustand 1), gefolgt von einem niedrigeren Aktivierungsenergiebalken für den Nukleophilangriff.
Praktische Hinweise
- Zur Förderung einer SN1-Reaktion wählt man polare, protische Lösungsmittel und versucht, eine gute Abgangsgruppe zu haben.
- Bei entgegengesetzten Beobachtungen (z. B. kein Racemisationsgrad, kein Umlagerungsprodukt) sollte geprüft werden, ob statt SN1 eine SN2-, E1- oder ein anderer Mechanismus vorliegt.
Insgesamt ist die SN1-Reaktion ein zentraler Mechanismus der organischen Chemie, wichtig zur Erklärung vieler Substitutionsprozesse, insbesondere wenn ionische Zwischenstufen und Umlagerungen eine Rolle spielen.