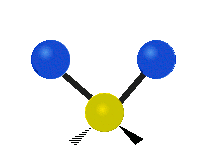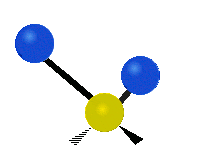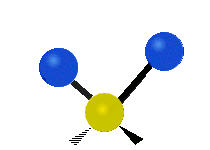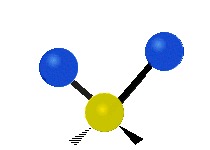
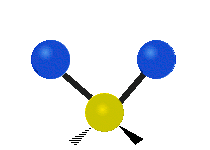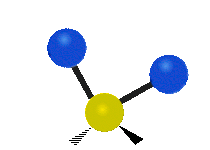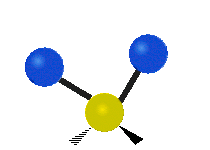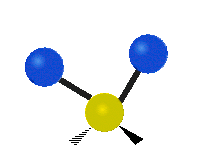
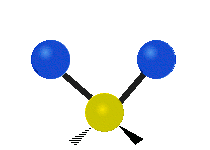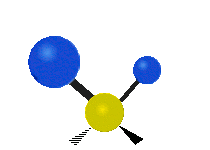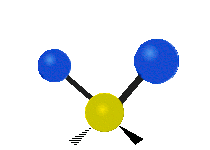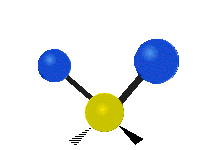
Molekülschwingungen sind eine von drei grundlegenden Bewegungsarten für Moleküle. Die beiden anderen sind die Translationsbewegung (wenn das ganze Molekül als Einheit in eine Richtung verschoben wird) und die Rotationsbewegung (wenn sich das Molekül wie ein Kreisel dreht). Bei Molekülschwingungen verändern Atome in einem Molekül ihre relative Lage zueinander: Bindungen „dehnen“ oder „biegen“ sich periodisch, ähnlich wie Kugeln, die durch Federn verbunden sind.
Was genau ist eine Schwingung?
Bei einer Schwingungsbewegung bewegen sich die Bindungen zwischen den Atomen und die Atome selbst hin und her. Das einfachste Beispiel ist das Dehnen (Streckung) einer Bindung zwischen zwei Atomen — das charakteristische Modell dafür ist der harmonische Oszillator. Bei zweiatomigen Molekülen (Diatome) gibt es genau eine Schwingungsart: das Strecken der Bindung. Beispiele für solche Diatome sind Wasserstoff H2, Stickstoff N2 und Sauerstoff O2.
Arten von Schwingungen
- Streckung (Stretch): Die Verbindungslinie zwischen zwei Atomen legt sich periodisch länger und kürzer.
- Biegung (Bend): Der Bindungswinkel zwischen Atomen ändert sich (z. B. bei gewinkelten Molekülen wie H2O).
- Innen- und Außenschwingungen: Bei größeren Molekülen können komplexe Bewegungen auftreten, bei denen mehrere Bindungen gleichzeitig mitwirken (Kombinationen von Streck- und Biegebewegungen).
Normale Moden und Freiheitsgrade
Jedes Molekül mit N Atomen hat insgesamt 3N Freiheitsgrade (je drei Raumrichtungen pro Atom). Davon sind:
- 3 Freiheitsgrade Translational (Gesamtverschiebung des Moleküls),
- bei nicht-linearen Molekülen 3 Freiheitsgrade Rotation, bei linearen Molekülen 2 Rotationsfreiheitsgrade,
- der Rest sind Schwingungsfreiheitsgrade: bei nicht-linearen Molekülen 3N − 6, bei linearen 3N − 5. Diese entsprechen den sogenannten normalen Schwingungsmoden (normal modes).
Beispiel: Ein Diatom (N = 2) hat 3·2 = 6 Freiheitsgrade → 3 Translations + 2 Rotation (für ein Diatom ist Rotation im Raum tatsächlich nur 2 unabhängig) = 5 → 1 Vibrationsmodus (3N − 5 = 1). Ein dreiatomiges lineares Molekül wie CO2 hat 3·3 − 5 = 4 normale Moden (eine symmetrische Streckung, eine antisymmetrische Streckung und zwei entartete Biegungen).
Spektroskopische Relevanz
Schwingungen haben typischerweise Energien im Bereich der Infrarot-Strahlung. Deshalb lässt sich mit der Infrarot (IR)-Spektroskopie die Schwingungsstruktur von Molekülen untersuchen. Wichtige Punkte:
- Für IR-aktive Schwingungen muss sich während der Bewegung das Dipolmoment des Moleküls ändern (Selektionsregel). Homonukleare Diatome wie H2, N2 oder O2 besitzen keinen permanenten Dipol und zeigen deshalb in der Regel keine starken IR-Banden beim Strecken – diese Moden können jedoch in der Raman-Spektroskopie beobachtet werden.
- Die harmonische Näherung beschreibt viele Grundzüge: Schwingungen sind quantisiert und haben diskrete Energieniveaus. Durch Anharmonizität entstehen Obertöne und Kombinationen (weiter entfernte Linien im Spektrum).
- IR- und Raman-Spektren sind oft komplementär: Manche Moden sind IR-aktiv, andere Raman-aktiv.
Vereinfachte Modelle und praktische Beispiele
Zur Beschreibung von Molekülschwingungen verwendet man oft einfache Modelle wie die Feder-Masse (harmonischer Oszillator) und berechnet daraus Frequenzen, die Rückschlüsse auf Bindungsstärken erlauben: je stärker die Bindung, desto höhere Schwingungsfrequenz.
Praktische Beispiele:
- Diatomische Gase (H2, N2, O2): haben eine einfache Streckschwingung; bei homonuklearen Diatomen ist diese häufig IR-inaktiv.
- Wasser (H2O): drei Schwingungsmoden (symmetrisches Strecken, antisymmetrisches Strecken, Biegen) mit typischen IR-Banden im mittleren Infrarot.
- Kohlenstoffdioxid (CO2): besitzt eine IR-aktive asymmetrische Streckschwingung und zwei entartete Biege-Moden; die symmetrische Streckschwingung ist aufgrund fehlender Dipolmomentänderung IR-inaktiv.
Warum sind Molekülschwingungen wichtig?
Sie liefern direkte Informationen über Bond-Längen und -stärken, sind Grundlage vieler Analysen in Chemie und Materialwissenschaft (z. B. Identifikation von funktionellen Gruppen) und spielen eine Rolle in Phänomenen wie Wärmeleitung, Reaktionsdynamik und optischen Eigenschaften von Materialien.
Kurz zusammengefasst: Molekülschwingungen sind periodische Bewegungen der Atome innerhalb eines Moleküls, beschrieben durch normale Moden. Sie sind quantisiert, liefern charakteristische Spektrallinien (vor allem im IR-Bereich) und erlauben Einsichten in die Struktur und Bindungsstärke von Molekülen.