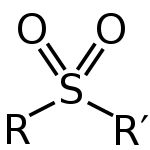
Ein Sulfon ist ein Molekül, das ein Schwefelatom trägt, das über je eine formale Doppelbindung zu zwei Sauerstoffatomen verfügt (Strukturformel allgemein: R–S(=O)2–R'). Zusätzlich ist der Schwefel über Einfachbindungen mit zwei organischen Resten verbunden. Die S=O-Bindungen lassen sich auch durch mesomere Grenzstrukturen beschreiben: die negative Ladung kann auf die Sauerstoffe delokalisiert und der Schwefel positiv partial aufgeladen sein. In formaler Oxidationszahl steht der Schwefel in Sulfonen typischerweise in der Oxidationsstufe +4.
Die Synthetische Hauptroute zu Sulfonen ist die Oxidation von Thioethern (Sulfiden). Übliche Oxidationsmittel sind organische Peroxy- oder Persäuren (z. B. mCPBA), Wasserstoffperoxid (H2O2) oder Oxone; die Oxidation verläuft häufig schrittweise vom Sulfid über das Sulfoxid (R–S(=O)–R') zum Sulfon (R–S(=O)2–R'). Alternativ lassen sich Sulfone auch über Reaktionen von Sulfonylchloriden (R–SO2Cl) mit geeigneten Nukleophilen bzw. Organometallverbindungen oder durch Einführung eines Sulfonylrests an ein C-Atom (z. B. als Teil von Addition–Eliminationssequenzen) herstellen.
Eigenschaften
- Polarität und Siedepunkt: Sulfone sind polar und zeigen oft hohe Schmelz‑ bzw. Siedepunkte im Vergleich zu vergleichbaren Kohlenwasserstoffen. Durch die polaren S=O‑Gruppen sind sie gute Lösungsmittel oder Zusatzstoffe in polaren Systemen.
- Stabilität: Sulfone sind thermisch und chemisch relativ stabil gegenüber vielen Säuren und Basen; sie lassen sich jedoch unter starken reduzierenden Bedingungen (z. B. Raney‑Nickel, starke Hydrierung) zu Sulfiden zurückführen.
- Spektroskopie: IR‑Spektren zeigen charakteristische starke S=O‑Bande(n) typischerweise in etwa 1300 und 1150 cm−1. In der NMR erscheinen α‑Protonen zu einem Sulfon stark deshielded.
Wichtige Reaktionen und Einsatzgebiete
Sulfone werden in vielen organischen Synthesen und industriellen Anwendungen verwendet. Beispiele:
- Julia‑Olefination: In der organischen Synthese dient das Sulfon als Vorstufe zur Bildung von Alkenen: ein sulfonylierter Carbanion greift ein Aldehyd an und nach Folgeumwandlungen entsteht ein Alken. Varianten wie die Julia–Kocienski‑Reaktion sind sehr verbreitet.
- Ramberg‑Bäcklund‑Reaktion: Umwandlung von α‑halogenierten Sulfonen in Alkenen durch Basen und Halogenierungsschritte.
- Desulfonylierungen: Sulfonylgruppen können unter bestimmten Bedingungen wieder entfernt werden (z. B. Reduktion), was sie zu nützlichen temporären Schutz‑ oder Aktivierungsgruppen macht.
- Lösungsmittel: Bestimmte Sulfone werden als Lösungsmittel eingesetzt. Ein bekanntes Beispiel ist Sulfolan (Tetrahydrothiophen‑1,1‑dioxid, auch Tetramethylenesulfone genannt), das in der Petrochemie und in der Elektrochemie wegen seiner hohen Polarität und thermischen Stabilität verwendet wird. Auch Dimethylsulfon (MSM, DMSO2) ist ein stabiles, polares kleines Sulfon.
- Polymere: Sulfon‑Einheiten treten in Hochleistungspolymeren wie Polysulfonen und Polyethersulfonen auf. Diese Werkstoffe zeichnen sich durch hohe Temperaturbeständigkeit, mechanische Festigkeit und chemische Beständigkeit aus und finden Anwendung in Membranen, Medizintechnik, Luft‑ und Raumfahrt sowie in Filtermaterialien.
- Pharma und Agro: Viele Arzneimittel und Agrochemikalien enthalten Sulfonylgruppen (oder Sulfone) als Teil ihrer Wirkstoffstruktur; die Sulfonylgruppe beeinflusst Lipophilie, Polarität und Metabolismus der Moleküle.
Spezielle reaktive Eigenschaften
- Die α‑Wasserstoffatome an einer Sulfon‑gebundenen C‑Position sind durch das electronenziehende Sulfon stark saurer als in einfachen Alkanen und können mit Basen deprotoniert werden. Diese Carbanionen sind synthetisch sehr nützlich (z. B. in der Julia‑Reaktion).
- Sulfonylchloride (R–SO2Cl) sind reaktive Zwischenstufen zur Einführung von Sulfonylgruppen, müssen aber wegen ihrer Reaktivität gegenüber Wasser und Nukleophilen mit Vorsicht gehandhabt werden.
Sicherheit und Umwelt
Viele Sulfone selbst sind relativ chemisch inert und weisen geringe akute Toxizität auf (konkrete Daten hängen jedoch vom Substituenten R ab). Reaktive Vorstufen wie Sulfonylchloride oder stark oxidierende Reagenzien können dagegen gefährlich sein. In der Handhabung sind standardmäßige Schutzmaßnahmen (Schutzbrille, Handschuhe, geeignete Lüftung) zu beachten. Für industrielle Anwendungen spielen außerdem Aspekte wie Bioabbaubarkeit und Entsorgung eine Rolle.
Zusammenfassend sind Sulfone eine wichtige und vielseitige Stoffklasse: Sie kombinieren eine ausgeprägte Polarität und Stabilität mit nützlichen chemischen Reaktivitäten (insbesondere durch aktivierte α‑Positionen) und finden breite Anwendung in Synthese, Lösungsmitteln, Materialien und Wirkstoffen.