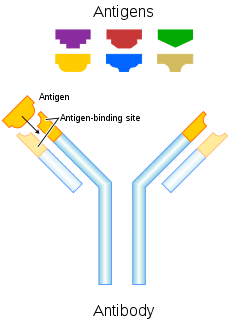
Antikörper (auch Immunglobuline genannt) sind große Y-förmige Proteine, die an der Oberfläche von Bakterien und Viren haften können. Sie finden sich im Blut oder anderen Körperflüssigkeiten von Wirbeltieren. Antikörper sind das Schlüsselelement im adaptiven Immunsystem.
Der Antikörper erkennt einen einzigartigen Teil des fremden Ziels, das so genannte Antigen. Jede Spitze des "Y" eines Antikörpers enthält eine Struktur (wie ein Schloss), die zu einer bestimmten schlüsselähnlichen Struktur auf einem Antigen passt. Dadurch werden die beiden Strukturen miteinander verbunden.
Mit Hilfe dieses Bindungsmechanismus kann ein Antikörper eine Mikrobe oder eine infizierte Zelle für den Angriff durch andere Teile des Immunsystems markieren oder sein Ziel direkt neutralisieren. Die Produktion von Antikörpern ist die Hauptfunktion der humoralen Immunität.
Jeder Antikörper ist anders. Sie sind alle darauf ausgelegt, nur eine Art von Antigen (in der Praxis bedeutet dies Virus oder Bakterien) anzugreifen. Zum Beispiel kann ein Antikörper, der die Pocken vernichten soll, weder die Beulenpest noch die Erkältung bekämpfen.
Obwohl die allgemeine Struktur aller Antikörper sehr ähnlich ist, ist dieser kleine Bereich an der Spitze des Proteins extrem variabel. Dies ermöglicht die Existenz von Millionen von Antikörpern mit unterschiedlichen Spitzenstrukturen. Jede dieser Varianten kann sich an ein anderes Antigen binden. Diese enorme Vielfalt von Antikörpern ermöglicht es dem Immunsystem, eine ebenso große Vielfalt von Antigenen zu erkennen.
Aufbau eines Antikörpers
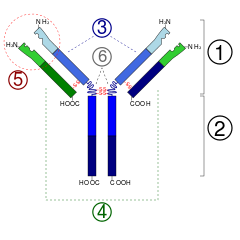
Antikörper bestehen aus vier Proteinketten: zwei identischen schweren (H‑Ketten) und zwei identischen leichten Ketten (L‑Ketten), die durch Disulfidbrücken verbunden sind. Man unterscheidet zwei funktionelle Bereiche:
- Fab‑Region (Fragment, antigen binding): die beiden Arme des Y, die die variablen Regionen (V‑Regionen) enthalten. Diese Bereiche bilden die Antigenbindungsstellen; in ihnen liegen die hochvariablen Schleifen, die sogenannten CDRs (complementarity determining regions).
- Fc‑Region (Fragment, crystallizable): der Schaft des Y, der konstante Regionen enthält und mit Rezeptoren auf Immunzellen (Fc‑Rezeptoren) sowie mit dem Komplementsystem interagiert. Über die Fc‑Region vermittelt der Antikörper Funktionen wie Opsonisierung und Aktivierung von Effektormechanismen.
Hauptfunktionen von Antikörpern
- Neutralisation: Antikörper blockieren Eintrittsstellen von Viren oder Toxinen, so dass diese Zellen nicht infizieren oder schädigen können.
- Opsonisierung: Antikörper bedecken Mikroorganismen und machen sie für Fresszellen (Phagozyten) leichter erkennbar.
- Aktivierung des Komplementsystems: Bestimmte Antikörper können das Komplementsystem auslösen, was zur Lyse von Mikroben oder zur verstärkten Entzündungsreaktion führt.
- ADCC (antibody‑dependent cellular cytotoxicity): über die Fc‑Region vermitteln Antikörper die Erkennung und Tötung von Zellen durch natürliche Killerzellen.
Antikörperklassen (Immunglobulin‑Isotype)
Beim Menschen gibt es verschiedene Klassen von Immunglobulinen, die sich in Struktur und Funktion unterscheiden:
- IgM: meist pentamere Form im Blut, erster Antikörper-Typ bei einer Neuinfektion; sehr effektiv bei Komplementaktivierung.
- IgG: wichtigste im Blut zirkulierende Klasse, langlebig, kann die Plazenta passieren und so den Fötus schützen; mehrere Subtypen (z. B. IgG1–4) mit unterschiedlichen Eigenschaften.
- IgA: vorherrschend in Schleimhäuten und Sekreten (Speichel, Tränen, Muttermilch) und wichtig für die mukosale Abwehr.
- IgE: beteiligt an Abwehr gegen Parasiten und an allergischen Reaktionen.
- IgD: vorwiegend auf der Oberfläche von B‑Zellen als Rezeptor vorhanden; Rolle noch nicht vollständig geklärt.
Entstehung und Diversität
Antikörperdiversität entsteht in B‑Lymphozyten durch mehrere genetische Mechanismen:
- V(D)J‑Rekombination: zufälliges Zusammenfügen verschiedener Genabschnitte für die variablen Regionen erzeugt viele Kombinationen.
- Somatische Hypermutation: nach Antigenkontakt werden in den Keimzentren der Lymphknoten gezielte Mutationen in den Antikörpergenen eingeführt; B‑Zellen mit höherer Affinität werden selektiert (Affinitätsreifung).
- Isotypwechsel (class switch recombination): ermöglicht es einer B‑Zelle, die gleiche Antigen‑Spezifität beizubehalten, aber die konstante Region zu wechseln (z. B. von IgM zu IgG oder IgA), um unterschiedliche Effektor‑Funktionen zu erlangen.
Bedeutung in Medizin und Diagnostik
- Impfungen: Nutzen die Fähigkeit des Körpers, Antikörper und Gedächtniszellen zu bilden, um langfristigen Schutz gegen Erreger aufzubauen.
- Diagnostische Tests: Antikörper‑Nachweise (z. B. ELISA, Western Blot, Schnelltests) zeigen, ob jemand Kontakt zu einem Erreger hatte oder eine Immunantwort entwickelt hat.
- Therapeutische Antikörper: Monoklonale Antikörper werden gezielt zur Behandlung von Krebs, Autoimmunerkrankungen, Infektionen und als Antitoxine eingesetzt.
- Passiver Schutz: Gabe von Antikörperpräparaten (Immunglobuline) kann sofortigen, aber vorübergehenden Schutz bieten, z. B. nach Exposition gegenüber bestimmten Erregern oder bei Immundefekten.
Klinische Aspekte und Störungen
Fehlregulationen des Antikörper‑Systems können zu Problemen führen:
- Autoantikörper: Antikörper gegen körpereigene Strukturen verursachen Autoimmunerkrankungen (z. B. rheumatoide Arthritis, Autoimmunthyreoiditis).
- Allergien: IgE‑vermittelte Reaktionen können zu Asthma, Heuschnupfen oder anaphylaktischem Schock führen.
- Immundefekte: Verminderte Antikörperproduktion (z. B. bei antikörperdefizienten Syndromen) führt zu wiederkehrenden Infektionen.
Zusammenfassung
Antikörper sind spezialisierte Proteine des adaptiven Immunsystems, die durch ihre enorme Vielfalt fremde Antigene erkennen und neutralisieren oder für andere Immunzellen markieren. Ihre unterschiedlichen Klassen und Funktionen machen sie zu zentralen Akteuren in Infektionsabwehr, Impfstrategie, Diagnostik und Therapie. Durch genetische Mechanismen erzeugt das Immunsystem die Vielfalt, die nötig ist, um eine sehr große Bandbreite von Krankheitserregern zu erkennen und zu bekämpfen.