Keratin: Struktur, Funktion und Vorkommen in Haar, Horn & Federn
Keratin: Aufbau, Funktionen und Vorkommen in Haar, Horn, Nägeln, Hufen und Federn – zähe Faserproteine, biologische Bedeutung und Anwendungen verständlich erklärt.
Keratine sind eine Familie von Faserproteinen. Keratin bildet bei Tieren das Haar, aber auch Hörner, Nägel, Hufe, Schalen, Schnäbel und Federn. Der Name kommt vom griechischen Wort keras, was "Horn" bedeutet.
Keratine sind zäh und unlöslich. Sie bilden die harten, aber nichtmineralischen Strukturen in Reptilien, Vögeln, Amphibien und Säugetieren. Eine ähnliche biologische Zähigkeit findet sich bei Chitin.
Aufbau und Typen
Keratine sind Polypeptide, die sich zu länger stabilen Strukturen zusammenlagern. Bei Säugetieren überwiegen die sogenannten Alpha-Keratine, deren Monomere eine charakteristische zentrale alpha-helikale "Stab"-Domäne besitzen. Diese Monomere paaren sich zu Heterodimeren (typischerweise ein Typ-I- mit einem Typ-II-Keratinderivat), die weiter zu Tetrameren und schließlich zu den feinen intermediären Filamenten (Durchmesser ≈ 10 nm) polymerisieren. Bei Vögeln und Reptilien sind häufig härtere Beta-Keratine (auch corneous beta-proteins genannt) vorhanden, die mehr beta-Faltblatt-Struktur aufweisen und dadurch besonders harte Hornschichten und Federn bilden.
Biochemische Eigenschaften
- Hoher Anteil an Cystein: führt zu Disulfidbrücken (S–S), die die mechanische Festigkeit und Dauerhaftigkeit erhöhen (z. B. in Haaren und Hörnern).
- Hydrophobe Aminosäurereste: sorgen für schlechte Löslichkeit in Wasser und Widerstand gegen viele Enzyme.
- Unlöslichkeit: Keratine sind in wässrigen Medien kaum löslich; sie lassen sich nur mit starken Denaturierern oder reduzierenden Agenzien (z. B. Mercaptoethanol) aufschließen.
- Abbaubarkeit: bestimmte Mikroorganismen und Pilze produzieren Keratinasen, Enzyme, die Keratin abbauen können — wichtig im Ökosystem und für industrielle Prozesse.
Bildung und Funktion im Körper
Keratin wird in spezialisierten Zellen gebildet, etwa in Keratinozyten der Epidermis, in Haarfollikeln sowie in den Zellen, die Nägel und Hornschichten produzieren. Die Umwandlung lebender Zellen zu toten, keratinisierten Schichten heißt Keratinisierung oder Korneifikation. Durch diese Prozesse entstehen barrierebildende und mechanisch belastbare Strukturen mit mehreren Funktionen:
- Mechanischer Schutz vor Reibung und Verletzungen (Haut, Hufe, Hörner).
- Barriere gegen Wasserverlust und gegen das Eindringen von Krankheitserregern (Hornschichten der Haut).
- Isolation und Temperaturregulation (Haarkleid, Federn).
- Spezialisierte Werkzeuge: Krallen, Schnäbel, Hufe, Barten (Baleen) ermöglichen unterschiedliche ökologische Nischen.
Vorkommen — Beispiele
- Mammalia: Haar, Nägel, Hoof- und Hornschichten (z. B. Kuhhorn), Wolle.
- Aves: Federn und Schnabelränder bestehen überwiegend aus Beta-Keratinen.
- Reptilien: Schuppen und Krallen sind keratinisiert.
- Amphibien: weniger ausgeprägte Keratinisierung, aber z. B. Mundwerkzeuge von Kaulquappen sind keratinreich.
- Andere: Baleen der Bartenwale und die Schuppen/Schichten vieler Wirbeltiere.
Genetik und evolutionäre Aspekte
Keratine werden von großen Genfamilien kodiert (KRT-Gene). Verschiedene Gene sind in unterschiedlichen Geweben exprimiert; Mutationen in bestimmten KRT-Genen können zu erblichen Haut- und Haarerkrankungen führen. Evolutionär führen Genverdopplungen und -divergenz zur Vielfalt der Keratintypen, die an verschiedene Lebensweisen (z. B. Gefieder, Fell, Hufe) angepasst sind.
Klinische Relevanz und Nutzung
- Erbkrankheiten: Mutationen in Keratin-Genen verursachen z. B. Epidermolysis bullosa simplex oder Nagel-Haar-Störungen; Symptome reichen von Blasenbildung bis zu brüchigem Haar.
- Dermatologie und Kosmetik: Keratinbehandlungen im Friseurhandwerk (z. B. Glättungs- und Pflegeprodukte) sowie Shampoos zur Stärkung von Haaren.
- Biotechnologie: Gewinnung von Keratin aus Nebenprodukten (z. B. Haar, Federn, Wolle) für Biomaterialien, Wundauflagen, Beschichtungen und Düngemittel.
- Ökologie/Industrie: Keratinabbau durch Mikroben spielt eine Rolle bei der Verwertung organischer Abfälle und bei der Bioremediation.
Zusammenfassung
Keratine sind vielseitige, hoch spezialisierte Strukturproteine, die in vielen Tiergruppen harte, schützende und funktionell wichtige Oberflächen bilden. Ihre molekulare Organisation (alpha- bzw. beta-Strukturen, Disulfidbrücken, intermolekulare Filamente) erklärt die mechanische Stabilität und chemische Resistenz dieser Gewebe. Sowohl in der Biologie als auch in Medizin und Technik sind Keratine deshalb von großer Bedeutung.
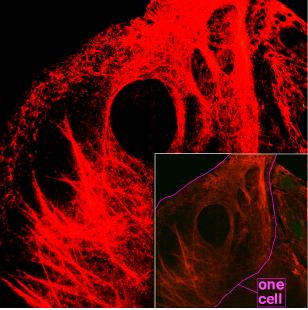
Mikroskopie von Keratinfilamenten im Inneren von Zellen.
Vielfalt der Tierverwendung
Keratine sind der Hauptbestandteil von Strukturen, die aus der Haut herauswachsen:
- die α-Keratine in den Haaren (einschliesslich Wolle), Hörnern, Nägeln, Klauen und Hufen von Säugetieren
- die härteren β-Keratine in den Schuppen und Krallen von Reptilien, ihren Panzern (Chelonia, wie z.B. Schildkröte, Schildkröte, Sumpfschildkröte) und in den Federn, Schnäbeln und Krallen von Vögeln. Diese Keratine werden hauptsächlich in Beta-Blättern gebildet. Beta-Blätter sind jedoch auch in α-Keratinen zu finden.
Bei Arthropoden wie Krustentieren bestehen Teile ihres Exoskeletts häufig aus Keratin, manchmal in Kombination mit Chitin.
Keratine kommen auch im Magen-Darm-Trakt vieler Tiere vor, darunter auch bei Spulwürmern (die ebenfalls eine äußere Schicht aus Keratin haben).
Obwohl es jetzt schwierig ist, sicher zu sein, wären die Schuppen, Krallen, ein gewisser Schutzpanzer und die Schnäbel von Dinosauriern mit ziemlicher Sicherheit aus einer Art Keratin zusammengesetzt gewesen.
Seide
Die von Insekten und Spinnen produzierten Seidenfibroine werden oft als Keratine klassifiziert, wobei unklar ist, ob sie phylogenetisch mit den Keratinen von Wirbeltieren verwandt sind.
Seide, die in Insektenpuppen sowie in Spinnennetzen und Eihüllen gefunden wird, hat auch gedrehte β-gefaltete Blätter, die in Fasern eingearbeitet sind, die zu größeren supermolekularen Aggregaten gewickelt sind.
Suche in der Enzyklopädie