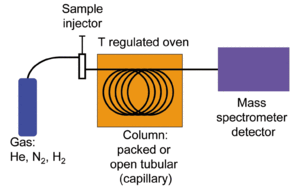
Die Gaschromatographie-Massenspektrometrie (GC-MS) kombiniert die Trennleistung der Gaschromatographie (GC) mit der chemischen Identifikationskraft der Massenspektrometrie (MS). Dadurch lassen sich in einer Probe einzelne Komponenten trennen, ihre Molekülstruktur ableiten und eindeutig identifizieren. Die Methode ist besonders geeignet für flüchtige und semi-flüchtige organische Verbindungen und wird in vielen Bereichen wie Forensik, Umweltanalyse, Lebensmittelsicherheit, klinischer Diagnostik und Sicherheitstechnik eingesetzt. Beispiele sind Drogennachweise, Brandursachenanalyse, Untersuchung von Pestiziden, Bestimmung von flüchtigen organischen Verbindungen (VOCs) und das Auffinden von Spurenelementen in stark angegriffenen Materialien.
Wie funktioniert GC-MS? — Ablauf in Schritten
Der typische Ablauf einer GC-MS-Analyse umfasst folgende Schritte:
- Probenahme und Probenvorbereitung: Extraktion, Reinigung und bei Bedarf Derivatisierung (um nichtflüchtige oder thermisch labile Substanzen GC-gängig zu machen).
- Injektion: Die Probe wird in den Gasstrom (Trägergas, z. B. Helium) eingeführt, oft mit split/splitless-Injektion oder durch Kopfraum-/Headspace-/SPME-Techniken für gasförmige Stoffe.
- Trennung in der GC: Auf einer kapillären Säule trennt eine stationäre Phase die Komponenten zeitlich (Retention). Die Temperatur wird meist programmiert, um Komponenten mit verschiedenen Siedepunkten nacheinander zu eluieren.
- Ionisierung: In der Massenspektrometrie werden Moleküle ionisiert, typische Methoden sind die Elektronenstoßionisation (EI) und die chemische Ionisation (CI). EI liefert reproduzierbare Fragmentierungsmuster, die für Bibliotheksabgleich wichtig sind.
- Massenanalyse und Detektion: Die erzeugten Ionen werden nach ihrem Masse-zu-Ladungs-Verhältnis (m/z) getrennt und detektiert. Gängige Analysatoren sind Quadrupole, Time-of-Flight (TOF) oder hochauflösende Systeme.
- Datenanalyse: Vergleich von Massenspektren mit Bibliotheken (z. B. NIST), Berücksichtigung von Retentionszeit und Fragmentmustern sowie quantitativer Nachweis mittels Kalibrierung und interner Standards.
Wichtige Komponenten und Begriffe
- Kapillarsäule: Entscheidet über Trennleistung; unterschiedliche stationäre Phasen werden je nach Probenmatrix gewählt.
- Trägergas: Inertgase wie Helium oder Wasserstoff transportieren die Probe durch die Säule.
- EI (Elektronenstoß): Liefert charakteristische Fragmentierungsdiagramme, die gut mit Spektrenbibliotheken abgeglichen werden können.
- CI (Chemische Ionisation): Schonendere Ionisation mit weniger Fragmentierung — nützlich zur Bestimmung des Molekulargewichts.
- GC-MS/MS: Tandem-Massenspektrometrie (z. B. für höhere Selektivität und niedrigere Nachweisgrenzen bei komplexen Matrizes).
Anwendungsgebiete
Die GC-MS ist sehr vielseitig. Wichtige Anwendungen sind:
- Forensik: Nachweis und Identifizierung von Betäubungsmitteln, Toxinen, Brandbeschleunigern und Explosivstoffrückständen (vgl. rollen für forensische Expertisen).
- Branduntersuchung: Analyse von Brandrückständen, um Brandbeschleuniger zu identifizieren.
- Umweltanalytik: Bestimmung von Pestiziden, PCB, VOCs und anderen Schadstoffen.
- Lebensmittelsicherheit: Rückstände von Pestiziden, Kontaminanten und Aromastoffe.
- Klinische Analytik & Toxikologie: Bestimmung von Arzneimitteln, Metaboliten und Giften im Blut oder Urin.
- Sicherheit & Flughafen-/Zollkontrolle: Erkennung von Substanzen im Gepäck oder an Menschen, z. B. Sprengstoffspuren.
- Archäologie & Materialanalyse: Identifizierung von Spurenelementen oder organischen Rückständen in stark verfallenen Proben.
Vorteile
- Hohe Selektivität und Spezifität: GC trennt Komponenten, MS liefert charakteristische Fragmentmuster — dadurch sichere Identifikation.
- Niedrige Nachweisgrenzen: Typisch im Bereich von pg–ng (abhängig von Probe und Gerät), besonders mit selektiven Techniken wie MS/MS.
- Quantifizierung: Präzise Bestimmung durch Kalibrierung und interne Standards.
- Breite Anwendbarkeit: Von forensischen Analysen bis zur Umweltüberwachung.
Beschränkungen und Besonderheiten
- Nicht für alle Substanzen geeignet: Sehr polare, nichtflüchtige oder thermisch labile Verbindungen müssen derivatisiert oder mittels LC-MS analysiert werden.
- Matrixeffekte: Störstoffe aus der Probe können die Analyse beeinflussen — sorgfältige Probenvorbereitung ist oft nötig.
- Interpretation: Bibliotheksabgleich allein reicht nicht immer — Retentionszeit, Ionratios und zusätzliche Standards erhöhen die Zuverlässigkeit. GC-MS gilt jedoch als sehr guter spezifischer Test, weil er das tatsächliche Vorhandensein einer Substanz bestätigen kann. Ein unspezifischer Test würde dagegen nur Kategorien von Substanzen anzeigen; dieser Unterschied hat Bedeutung, da ein unspezifischer Test zwar statistisch gesehen Hinweise geben kann, aber zu einer falsch-positiven Identifizierung führen könnte.
Qualitätssicherung
Validierung, regelmäßige Kalibrierung, Einsatz von Qualitätskontrollen und die Verwendung zertifizierter Referenzmaterialien sind wichtig, um verlässliche Ergebnisse zu gewährleisten. Für forensische und sicherheitsrelevante Anwendungen sind dokumentierte Arbeitsabläufe und Nachweisprotokolle unerlässlich.
Weiterentwicklungen
Moderne Varianten wie GC-MS/MS, GC-TOF-MS oder hochauflösende Massenspektrometrie erweitern die Leistungsfähigkeit (höhere Selektivität, schnellere Datenerfassung, bessere Massengenauigkeit) und erschließen weitere Einsatzgebiete, z. B. in der Metabolomforschung oder bei komplexen Umweltscreenings.
Zusammenfassend ist die GC-MS eine leistungsfähige, weit verbreitete Methode zur Identifizierung und Quantifizierung organischer Verbindungen. Ihre Kombination aus chromatographischer Trennung und massenspektrometrischer Identifikation macht sie besonders wertvoll in Bereichen, in denen Zuverlässigkeit und Nachweisbarkeit entscheidend sind.